向一定量的Fe、FeO和Fe2O3的混合物中加入140 mL5mol/L的稀硝酸,恰好使混合物完全溶解,放出2.24 L NO(标准状况),往所得溶液中加入KSCN溶液,无红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为 ( )
| A.0.24 mol | B.0.21 mol | C.0.25 mol | D.0.14 mol |
进行物质导电性实验测定时,按照图a、图b分别接通线路,下列叙述正确的是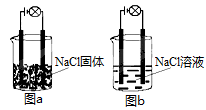
| A.NaCl是电解质,图a、图b灯泡均会发光 |
| B.图a灯泡不会发光,NaCl固体中不含Na+、Cl— |
| C.NaCl溶液在通电后发生:NaCl═Na+ +Cl— |
| D.通电前图b溶液由大量H2O、Na +、Cl—构成 |
下列有关叙述正确的是
| A.电泳现象可证明胶体带电荷 |
| B.胶体是一种纯净物 |
| C.胶体属于介稳体系 |
| D.将饱和氯化铁溶液滴入氢氧化钠溶液中制备氢氧化铁胶体 |
下列各组物质分类正确的是
| 酸 |
碱 |
盐 |
氧化物 |
|
| A |
硫酸 |
纯碱 |
硫酸钙 |
氧化铁 |
| B |
盐酸 |
烧碱 |
纯碱 |
氧化钙 |
| C |
碳酸 |
硫酸钙 |
碳酸钠 |
干冰 |
| D |
干冰 |
苛性钠 |
食盐 |
石灰石 |
下列叙述中错误的是
| A.阿伏加德罗常数的数值与12g12C所含的碳原子数相等 |
| B.在0.5mol Na2SO4中,含有的Na+数约是6.02×1023 |
| C.等物质的量的O2与O3,所含氧原子数相等 |
| D.摩尔是物质的量的单位 |
下列关于金属性质的叙述中正确的是
| A.钠与氧气反应时,产物是由O2的用量决定的 |
| B.铝箔在空气中受热可以熔化且会发生剧燃烧 |
| C.金属与非金属单质发生反应时,被氧化的一定是金属 |
| D.铁丝不论在空气还是纯氧中都不会燃烧 |