关于原电池的叙述正确的是
| A.原电池工作时,正极和负极上不一定都发生氧化还原反应 |
B.xLi+Li1-xNiO2 LiNiO2放电时此电池的负极材料是Li1-xNiO2 LiNiO2放电时此电池的负极材料是Li1-xNiO2 |
| C.在铅、银和盐酸构成的原电池工作时,铅板上有5.175 g铅溶解,正极上就有1120 mL(标准状况)气体析出 |
| D.在理论上可将该反应:CH4(g)+2O2(g)→CO2(g)+H2O(l) ΔH<0,设计成原电池 |
下列溶液中各微粒的浓度关系正确的是
| A.0.1 mol·L-1 NaHSO4溶液中:[Na+]>[SO42-]>[H+]>[OH-] |
| B.0.1 mol·L-1Na2S溶液中:2[Na+]=[S2-]+[HS-]+[H2S] |
| C.0.1 mol·L-1 NaHCO3溶液中:[Na+]+[H+]=[HCO3-]+2[CO32-]+[OH-] |
| D.等体积、等物质的量浓度的乙酸溶液和氢氧化钠溶液混合后:[Na+]=[CH3COO-]>[H+]=[OH-] |
下列化学反应式书写正确的是
A.制取氢氧化铁胶体的化学方程式为FeCl3+3H2O Fe(OH)3(胶体)+3HCl Fe(OH)3(胶体)+3HCl |
B.亚硫酸在溶液中的电离方程式为H2SO 2H++SO32- 2H++SO32- |
C.NaHCO3水解的离子方程式为HCO3-+H2O CO32-+H3O+ CO32-+H3O+ |
| D.电子工业印刷电路反应式为2Fe3++Cu=Cu2++2Fe2+ |
pH=1的两种一元酸HX与HY溶液,分别取50 mL加入足量的镁粉,充分反应后,收集到H2体积分别为V(HX)和V(HY)。若V(HX)>V(HY),则下列说法正确的是
| A.HX可能是强酸 |
| B.HX的酸性比HY的酸性弱 |
| C.两酸的浓度大小[HX]<[HY] |
| D.pH=1的两种一元酸均稀释100倍,稀释后两溶液的pH均为3 |
在相同的温度下,100 mL 0.01 mol·L-1醋酸溶液与10 mL 0.1 mol·L-1醋酸溶液相比较,下列数值中前者大于后者的是
| A.中和时所需氢氧化钠的物质的量 |
| B.H+的物质的量浓度 |
| C.电离平衡常数K |
| D.H+的物质的量 |
HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是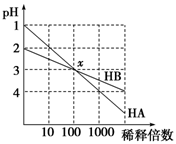
| A.HA是一种强酸 |
| B.x点,[A-]=[B-] |
| C.HB是一种弱酸 |
| D.原溶液中HA的物质的量浓度为HB的10倍 |