已知:①卤代烃可以和某些金属反应生成烃基金属有机化合物 。后者又能与含羰基( )的化合物反应生成醇:
。后者又能与含羰基( )的化合物反应生成醇: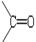
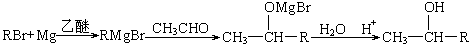
②苯在AlCl3催化下能与酰卤发生如下反应: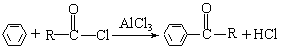
有机物E可由下述路线合成: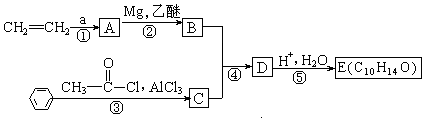
E与硫酸共热到适当温度可得到F和G。F分子中所有碳原子均可共处于同一平面上,G中只含有一个甲基。回答下列问题:
(1)C、D的结构简式分别是:C ,D 。
(2)G中核磁共振氢谱中氢原子的类型有 种。
(3)写出F形成高聚物反应的化学方程式: 。
(4)写出下列反应的化学方程式:
① ,
④  。
。
(5)E′是E的同分异构体且与E属同一类别。若E′不能从羰基化合物直接加氢还原得到,则E′可能的结构简式为(有几种写几种,下同) ;若E′能被催化氧化生 成醛,且E′与浓硫酸共热不能得到碳链不变的烯烃,E′为苯的一取代物,则E′可能的结构简式为 。
成醛,且E′与浓硫酸共热不能得到碳链不变的烯烃,E′为苯的一取代物,则E′可能的结构简式为 。
在0.5molH2S中,约含有个氢原子,共有mol原子,其质量为克,在标况下体积为L。
现有以下物质:①NaCl晶体②液态(纯)H2SO4 ③液态的(纯)醋酸 ④汞(金属)⑤纯蔗糖(C12H22O11) ⑥酒精(C2H5OH) ⑦熔化的KNO3,请回答下列问题(用序号):
(1)以上物质中能导电的是;
(2)以上物质中属于电解质的是;
(3)以上物质中属于非电解质的是。
某银白色固体A露置在空气中会被氧化成白色固体B;点燃A,火焰呈黄色,生成浅黄色固体C;A、B、C均可跟无色液体D反应,生成碱性物质E;其中A和D反应时还会生成可燃性气体F,C跟D反应时则可生成另一种气体G;F和G混合后遇火可剧烈反应而发生爆炸并生成D。
(1)写出下列物质的化学式:C,D,E。
(2)写出A与D反应的离子方程式:。
(3)写出C与D反应的化学方程式:。
(4)写出B与D反应的化学方程式:。
某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
| 检测次数 |
溶液中检测出的物质 |
| 第一次 |
KCl、K2SO4、Na2CO3、NaCl |
| 第二次 |
KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 |
Na2SO4、KCl、K2CO3、NaCl |
(1)三次检测结果中第次检测结果不正确。
(2)检测时,为了确定溶液中是否存在SO42-和CO32-:
第一,向溶液滴加溶液(填化学式),其目的是。
第二,继续加入过量的该溶液,其目的是。
第三,再向溶液中加入溶液(填化学式),确定离子的存在,其离子反应方程式为。
将1mol/L的FeCl3溶液逐滴滴入沸水中,液体变为色,得到的是;反应的化学方为。向其中逐滴加入稀硫酸至过量,现象是,原因是。