据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实。2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) 下列叙述错误的是
CH3CH2OH(g)+3H2O(g) 下列叙述错误的是
| A.使用Cu-Zn-Fe催化剂可大大提高生产效率 |
| B.反应需在300℃进行可推测该反应是吸热反应 |
| C.充入大量CO2气体可提高H2的转化率 |
| D.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率 |
某同学仿照“喷泉”实验的原理,在实验室中做了一个“喷烟”实验,如图所示。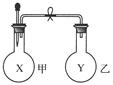
他在甲、乙两个烧瓶中分别充入X、Y两种无色气体;在胶头滴管中盛有含酚酞的NaOH溶液,实验时将胶头滴管内的液体挤入甲烧瓶内,然后打开止水夹,便可看到甲烧瓶中的导管口喷出白色的烟,同时甲烧瓶中的溶液颜色逐渐变浅。若已知X、Y是HCl、NH3、Cl2、O2、CH4、SO2、NO七种气体中的两种,则下列判断中,正确的是( )
| A.X是NH3,Y是HCl | B.X是Cl2,Y是CH4 |
| C.X是SO2,Y是O2 | D.X是NO,Y是O2 |
新华网酒泉9月20日电:由我国独立研制的“长征”系列运载火箭是中国航天的主力运载工具,自1996年10月以来,已连续进行366次成功发射。若某火箭推进器中的燃料是液态偏二甲基肼[(CH3)2N—NH2],氧化剂是N2O4,发生的反应可写为:(CH3)2N—NH2+2N2O4===3N2↑+2CO2↑+4H2O↑。下列有关说法不正确的是( )
| A.火箭点火后瞬间,逸出红棕色气体是NO2 |
| B.偏二甲基肼[(CH3)2—N—NH2]与均二甲基肼[CH3NH—NH—CH3]沸点不相同 |
| C.每生成3 mol氮气,转移电子的物质的量为16 mol |
| D.在宇宙飞船船舱中比在地球上更容易做过滤实验 |
较活泼的金属锌与不同浓度的HNO3反应时,可得到不同价态的还原产物。如果起反应的锌和HNO3的物质的量之比为4 ∶10,则HNO3的还原产物可能为( )
| A.NO2 | B.NO | C.N2O | D.NH4NO3 |
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3)反应原理是:2FeSO4Fe2O3+SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,依次将气体通过盛有(Ⅰ)BaCl2溶液、(Ⅱ)X溶液、(Ⅲ)NaOH溶液的三个装置。则下列对该方案的评价中正确的是( )
| A.(Ⅰ)中会生成BaSO3、BaSO4两种沉淀 |
| B.可将(Ⅰ)中的BaCl2溶液改为Ba(NO3)2溶液 |
| C.(Ⅱ)所盛X应为品红溶液 |
| D.(Ⅲ)的作用是检验生成的SO2气体 |
无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100 mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )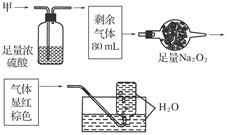
| A.NH3、NO2、N2 | B.NH3、NO、CO2 |
| C.NH3、NO2、CO2 | D.NO、CO2、N2 |