已知反应:① 2C(s)+O2(g)=2CO(g) ΔH= – 221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH= – 57.3 kJ·mol-1
下列结论正确的是( )
| A.碳的燃烧热为△H = –110.5 kJ·mol-1 |
| B.反应①的△H < 0,△S > 0,则△G < 0,在任意温度下反应可自发进行 |
| C.反应①中反应物的总键能大于生成物的总键能 |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出热量大于57.3 kJ |
在下列平衡体系中,保持温度一定时,改变某物质的浓度,混合气体的颜色会改变;改变压强时,颜色也会改变,但平衡并不移动,这个反应是
A.2NO+O2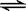 2NO2 2NO2 |
B.N2O4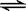 2NO2 2NO2 |
C.Br2(g)+H2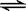 2HBr 2HBr |
D.6NO+4NH3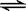 5N2+3H2O 5N2+3H2O |
下列按纯净物、混合物、电解质和非电解质顺序排列的是
| A.盐酸、空气、醋酸、干冰 |
| B.冰醋酸、福尔马林、硫酸钠、乙醇 |
| C.蛋白质、油脂、苛性钾、石灰石 |
| D.胆矾、漂白粉、氯化钾、硫酸钡 |
对于反应A(g)+3B(g) 2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
A、v(A)="0.01" mol/(L•s) B、v(B)="0.02" mol/(L•s)
C、v(B)=0.60mol/(L•min) D、v(C)=1.0mol/(L•min)
已知:H2(g)+F2(g) ===2HF(g) △H=-270kJ/mol,下列说法正确的是
| A.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ |
| B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ |
| C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量 |
| D.2mol氟化氢气体分解成1mol的氢气和1mol的氟气放出270kJ热量 |
相同温度下,有下列三个热化学方程式:
(1)2H2(l)+O2(g)===2H2O(l)△H1= -Q1 kJ• mol-1
(2)2H2(g)+O2(g)="==" 2H2O(l)△H1= -Q2 kJ• mol-1
(3)2H2(l)+O2(g)===2H2O(g)△H1= -Q3 kJ• mol-1
则Q1、Q2、Q3的关系表示正确的是
| A.Q1=Q2<Q3 | B.Q2 > Q1 >Q3 | C.Q3> Q2> Q1 | D.Q1=Q2=Q3 |