在一定条件下,固定容积的密闭容器中反应:2NO2(g)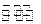 O2(g) + 2NO(g) —Q(Q>0),达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是()
O2(g) + 2NO(g) —Q(Q>0),达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是()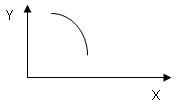
| A.当X表示温度时,Y表示NO2的物质的量 |
| B.当X表示压强时,Y表示NO2的转化率 |
| C.当X表示反应时间时,Y表示混合气体的密度 |
| D.当X表示NO2的物质的量时,Y表示O2的物质的量 |
某K2CO3样品中含有Na2CO3、KNO3和Ba(OH)2三种杂质中的一种或两种。现将13.8克样品加入入足量水,样品全部溶解,再加入过量的CaCl2溶液,得到9克沉淀。对样品所含杂质的正确判断是()
| A.一定含有KNO3 | B.一定含有KNO3,可能含有Na2CO3 |
| C.一定不含Ba(OH)2,可能含有KNO3 | D.一定不含Na2CO3和Ba(OH)2 |
下列溶液中有关判断正确的是()
A.常温下pH = 2的HA溶液与pH = 12的MOH溶液任意比混合:
C (H+) + c (M+) =" c" (OH-) + c (A-)
B.pH相等的CH3COONa、 NaOH和Na2CO3三种溶液:
C (NaOH) < c (CH3COONa) < c (Na2CO3)
C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:
C (CH3COO-) + 2c (OH-) =" 2c" (H+) + c (CH3COOH)
D. 0.1 mol / L的NaHA溶液,其pH = 4:c (HA-) > c (H+) > c (H2A) > c (A2-)
取0.2 mol / L HX溶液与0.2 mol / L NaOH溶液等体积混合(忽略混合后溶液体积变化),测得混合溶液的pH = 8,则下列说法正确的是()
| A.混合溶液中由水电离出的c (OH-)小于0.2 mol / LHX溶液中由水电离出的c(H+) |
| B.c (Na+) =" c" (X-) + c (HX) =" 0.2" mol / L |
| C.c (Na+) — c (X-) = 9.9×10-7mol /L |
| D.c (OH-) — c (HX) = c(H+) = 10-8 mol / L |
室温下,某无色溶液中由水电离出来的H+和OH-浓度的乘积为10-24,则此溶液中可能大量共存的离子组是()
| A.HCO3-、Al3+、Na+、SO42- | B.I-、NO3-、K+、NH4+ |
| C.MnO4-、Cl-、SO42-、K+ | D.SiO32-、SO32-、Na+、Cl- |