下列各项内容中,排列顺序正确的是
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3
②相同物质的量浓度的下列溶液中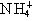 的浓度:(NH4)2SO4>(NH4)2CO3>NH4Cl
的浓度:(NH4)2SO4>(NH4)2CO3>NH4Cl
③微粒半径:K+>S2->F-
④给出质子的能力:CH3COOH>C2H5OH>H2O
⑤氢化物的沸点:H2Se>H2S>H2O
| A.①③ | B.②④ | C.①② | D.③⑤ |
在两份体积相同的氢氧化钠和稀硫酸溶液中分别加入过量铝粉,充分反应后,在相同状况下,若放出氢气的体积相同,则该氢氧化钠溶液与硫酸溶液的物质的量浓度之比为
| A.3:1 | B.1:3 | C.2:3 | D.3:2 |
某无色溶液可能由Na2CO3、MgCl2、NaHCO3、BaCl2中的一种或几种混合而成。取少量该溶液加入NaOH溶液出现白色沉淀;另取少量该溶液加入稀H2SO4也出现白色沉淀,并放出气体。据此分析,下述组合判断正确的是: ①肯定有BaCl2 ②肯定有MgCl2 ③肯定有NaHCO3 ④肯定有NaHCO3或Na2CO3 ⑤肯定没有MgCl2
| A.①②③ | B.①③ | C.②④ | D.①③⑤ |
下列各组中的离子,能在溶液中大量共存的是:
| A.K+、H+、SO42-、OH- | B.Na+、Ca2+、CO32-、NO3- |
| C.Na+、H+、Cl-、CO32- | D.Na+、Cu2+、Cl-、SO42- |
a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知
(1)a、c均能与稀硫酸反应产生氢气
(2)b和d的硝酸盐反应,置换出d单质;
(3)c与强碱溶液反应放出气体;
(4)c、e在冷浓硝酸中发生钝化。由此可判断a、b、c、d、e依次是
| A.Fe、Cu、Al、Ag、Mg | B.Mg、Cu、Al、Ag、Fe |
| C.Al、Cu、Ag、Mg、Fe | D.Mg、Ag、Al、Cu、Fe |
X、Y、Z、W有如下图所示的转化关系,则X、Y可能组合是:
| ① |
② |
③ |
④ |
|
| X |
C |
AlCl3 |
Fe |
Na2CO3 |
| Y |
CO |
Al(OH)3 |
FeCl2 |
NaHCO3 |
A.①②③ B.①③ C.③④ D.①②④