某溶液由Na+、Cu2+、Ba2+、Fe3+、AlO2-、CO32-、SO42-、Cl-中的若干种离子组成,取适量该溶液进行如下实验: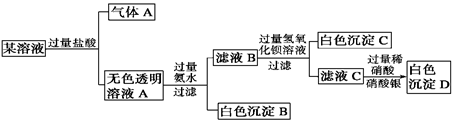
下列说法不正确的是 ( )
| A.原溶液中一定存在Na+、AlO2-、CO32-、SO42-离子 |
B.气体A的化学式是CO2,其电子式为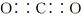 |
| C.原溶液中一定不存在的离子是Cu2+、Ba2+、Fe3+ |
| D.生成沉淀B的离子方程式为:Al3++3OH-===Al(OH)3↓ |
电子表所用电池的电极材料为Zn与Ag2O,电解质溶液为KOH溶液,电极反应为:Zn+2OH--2e-=Zn(OH)2; Ag2O+H2O+2e-=2Ag+2OH-
总反应为:Zn+Ag2O+H2O=2Ag+Zn(OH)2,下列判断正确的是
| A.锌为正极,氧化银为负极 |
| B.锌发生氧化反应,氧化银发生还原反应 |
| C.使用过程中,电流由Zn沿导线流向Ag2O |
| D.工作时,正极区的pH变小 |
下列分子结构图中的大黑点表示原子序数小于10的元素的“原子实”(指原子除去最外层电子的剩余部分),小黑点表示没形成共价键的最外层电子,短线表示共价键。其中分子结构图与化学式关系错误的是
A.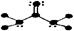 (C3H4O) (C3H4O) |
B. (HCN) (HCN) |
C.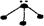 (NH3) (NH3) |
D.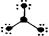 (BF3) (BF3) |
如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,则下列叙述中正确的是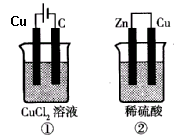
| A.产生气体的体积:①>② |
| B.溶液的pH变化:①不变②增大 |
| C.①和②中铜电极均失电子 |
D.电极反应式:①中阳极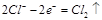 ②中负极 ②中负极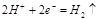 |
甲、乙两种金属性质比较:①甲的单质熔、沸点比乙的低;②常温下,甲能与水反应放出氢气而乙不能;③最高价氧化物对应的水化物碱性比较,乙比甲的强;④甲、乙作电极,稀硫酸为电解质溶液组成原电池,乙电极表面产生气泡。上述项目中能够说明甲比乙的金属性强的是
| A.①② | B.②④ | C.②③ | D.①③ |
已知一定温度时:N2(g)+3 H2(g) 2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入3mol H2和1mol N2,达到平衡时放出热量为Q,则下列关系式中正确的是
2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入3mol H2和1mol N2,达到平衡时放出热量为Q,则下列关系式中正确的是
| A.Q=92 kJ | B.Q< 92 kJ | C.Q> 92 kJ | D.Q<92×2 kJ |