(10分)工业上冶炼钛主要以钛铁矿、金红石(含TiO2大于96%)等为原料生产。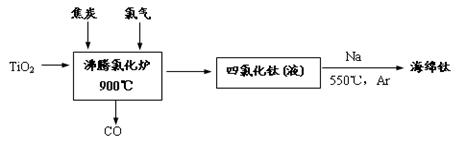
(1)由金红石为原料采用亨特(Hunter)法生产钛的流程如下:
①沸腾氯化炉中反应的化学方程式为:
②已知:Ti(s) +2Cl2(g) = TiCl4(l) △H = -804.2kJ/mol;
2Na(s) +Cl2(g) =" 2NaCl(s) " △H = -882.0kJ/mol
Na(s) =" Na(l) " △H ="2.6" kJ/mol
请写出用液态钠与四氯化钛置换出钛的热化学方程式
③海绵钛破碎后用0.5%~1.5%的盐酸洗涤,再用蒸馏水洗涤至中性,用盐酸洗涤的目的是 。
(2)科学家从电解冶炼铝的工艺得到启发,找出了冶炼钛的新工艺。试回答下列有关问题。
①TiO2直接电解法(剑桥法)生产钛是一种较先进的方法,电解质为熔融的氯化钙,原理如图所示,在阴极,被还原的Ca进一步还原TiO2获得钛,则在阴极所发生的反应为: 。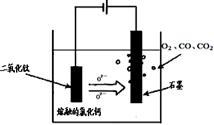
②SOM技术是一种绿色环保先进技术,阳极用金属陶瓷,并用固体氧离子隔膜将两极产物隔开,只允许氧离子通过,在电解过程中阳极通入某种还原性气体,可防止CO、CO2污染物产生,通入的气体若是H2,则阳极电解反应式为 。
试计算下列溶液的pH(均在25 ℃时):
(1)0.1 mol·L-1 NaOH溶液与0.1 mol·L-1 Ba(OH)2溶液等体积相混后溶液的pH为_____。
(2)将0.1 mol·L-1盐酸与0.6 mol·L-1Ba(OH)2溶液等体积相混后溶液的pH为________。
(3)将0.1 mol·L-1的稀H2SO4稀释1010倍后,溶液中c(H+)∶c( )=______________。
)=______________。
某学生在实验室测定溶液的pH时,先将pH试纸用蒸馏水润湿后再进行测定,其测定结果是否一定有误差?_____________,理由是_______________________________________。若用此方法分别测定c(H+)相等的H2SO4和H3PO4的pH,误差较大的是_____________,理由是_______________________________________。
如图4-6所示,甲是刚浸过Na2SO4溶液的滤纸,A、B两铜片通过导线连接电源两极,在铜片间的滤纸上滴一滴KMnO4溶液,通电一段时间后,发现A、B间紫红色圆点向A移动了一段距离,则与A相连的是电源的 极,可发现滤纸的 极边沿附近有 色出现。
某地的酸雨中,含c(Na+)=7.0×10-6 mol·L-1,c(Cl-)=4.5×10-5 mol·L-1,c(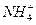 )=2.3×10-5 mol·L-1,c(
)=2.3×10-5 mol·L-1,c(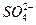 )=2.5×10-6 mol·L-1,则该地酸雨的pH约为。
)=2.5×10-6 mol·L-1,则该地酸雨的pH约为。
设水的电离平衡线如图3-4所示:(1)若以A点表示20 ℃时水在电离平衡时的离子浓度,当温度上升到100 ℃时,水的电离平衡状态到B点。则此时水的离子积______从增大到______。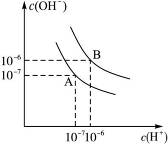
图3-4
(2)将100 ℃时pH=8的Ba(OH)2溶液与pH=5的稀H2SO4混合,并保持100 ℃的恒温。欲使混合液的pH=7,则Ba(OH)2与稀H2SO4的体积比为(二者混合后体积假设为二者体积之和)。