浓盐酸和氯酸钾的反应如下:KClO3 + 6HCl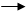 KCl + 3Cl2
KCl + 3Cl2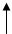 + 3H2O其中发生氧化反应的氯原子和发生还原反应的氯原子的质量比是( )
+ 3H2O其中发生氧化反应的氯原子和发生还原反应的氯原子的质量比是( )
| A.1∶6 | B.1∶5 | C.5∶1 | D.6∶1 |
下列有关电解质的说法正确的是()
| A.CO2、SO2、NH3、Na2O溶于水能导电,所以它们是电解质 |
| B.BaSO4、AgCl在水中溶解度很小,所以是弱电解质 |
| C.向醋酸溶液中加入氢氧化钠固体,溶液导电性增强 |
| D.向氨水中加水后,溶液中所有离子浓度都减小 |
下列有关说法正确的是()
| A.工业生产硫酸时,接触室中采用高温高压条件都能提高SO2和O2的转化率 |
| B.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能消毒杀菌又能净水 |
| C.阴离子交换树脂可以除去硬水中的Ca2+、Mg2+ |
| D.工业上电解熔融AlCl3可制金属铝 |
将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100 mL 4.40 mol/L盐酸中,充分反应后产生896 mL H2(标准状况),残留固体1.28 g。过滤,滤液中无Cu2+。将滤液加水稀释到200 mL,测得其中c(H+)为0.400 mol/L。已知Fe + 2Fe3+= 3Fe2+,Cu + 2Fe3+= 2Fe2++Cu2+。则原混合物中单质铁的质量是()
| A.2.4 g | B.3.36 g | C.5.60 g | D.10.08 g |
天宫一号搭载的长征二号火箭使用的主要燃料是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R + 2N2O4=3N2 + 4H2O + 2CO2,下列叙述错误的是()
| A.此反应可在瞬间产生大量高温气体,推动火箭飞行 |
| B.此反应是氧化还原反应,N2O4做还原剂 |
| C.此反应是氧化还原反应,偏二甲肼做还原剂 |
| D.此反应中R的分子式为C2H8N2 |
下面有关硅的叙述中,正确的是()
| A.硅原子既不易失去电子又不易得到电子,所以既不能作氧化剂,又不能作还原剂。 |
| B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位。 |
| C.硅的化学性质不活泼,在自然界中可以游离态存在。 |
| D.硅在电子工业中,是最重要的半导体材料。 |