石膏是一种节能建筑材料。某石膏样品是由二水石膏(CaSO4·2H2O)、半水石膏(CaSO4·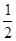 H2O)、无水石膏(CaSO4)三种成分组成,各组分含量可用下列方法测定。
H2O)、无水石膏(CaSO4)三种成分组成,各组分含量可用下列方法测定。
①称取8.70 g该石膏试样,在400℃干燥失去全部结晶水,质量变为8.16 g。
②再称取8.70 g的该石膏试样,加入80%的酒精溶液,使CaSO4完全水化成CaSO4·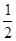 H2O,此时,其它两组分与酒精溶液不起作用;将试样取出干燥后称量,试样质量变为8.97 g。
H2O,此时,其它两组分与酒精溶液不起作用;将试样取出干燥后称量,试样质量变为8.97 g。
③在②中所得8.97 g试样中加入蒸馏水,使全部的CaSO4·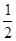 H2O都水化成CaSO4·2H2O,取出干燥后再次称量,质量变为10.32 g。
H2O都水化成CaSO4·2H2O,取出干燥后再次称量,质量变为10.32 g。
(1)试样中结晶水的质量分数为__________________(用小数表示)。
(2)试样中无水石膏(CaSO4)的物质的量为____________ mol。
(3)试样中三种石膏的物质的量之比为:
n(CaSO4·2H2O)∶n(CaSO4·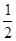 H2O)∶n(CaSO4)= __________________。
H2O)∶n(CaSO4)= __________________。
0.2mol有机物与1.6molO2在密闭容器中恰好完全反应后的产物为CO2和H2O(g),产物先通过足量的浓H2SO4质量增加21.6g,再通过碱石灰被完全吸收,质量增加44g。试推断该有机物的分子式(要求写出过程)
写出该有机物可能有的同分异构体的结构简式,并用系统命名法命名
将气体A、B置于容积为5L的密闭容器中,发生如下反应:3A(g) +B(g)  2C(g)+2D(g),反应进行到10s末,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol,则:
2C(g)+2D(g),反应进行到10s末,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol,则:
(1)求用C来表示的该反应的速率;
(2)求反应前A的物质的量浓度;
(3)反应10s后,求B物质的转化率。
(请在答题纸上写出本题详细的解题过程)
有一硫酸和硝酸的混合溶液,取出其中的10mL,加入足量 BaCl2溶液,将生成的沉淀滤出洗净,烘干称得其质量为9.32g;另取此溶液10mL与4.00 mol·L-1的NaOH溶液25mL恰好完全中和。求:
①混合液中硫酸的物质的量浓度是多少?
②混合液中硝酸的物质的量浓度又是多少?
③若将9.6g铜片投入到10mL的混合溶液中,则标况下能生成气体多少毫升?
(1)某温度下,在一密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。分析有关数据,写出X、Y、Z反应的化学方程式。
(2)某温度下,在另一密闭容器中充入2molX和3molY,然后按(1)中的化学方程式进行反应,当达到化学平衡时,测得Z的物质的量分数为25%,求平衡时X的转化率。
如图所示,当关闭阀门K时,向甲中充入1.5 mol A、3.5 mol B,向乙中充入3 mol A、7 mol B,起始时,甲、乙体积均为V L。在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:3A(g)+2B(g)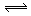 C(g)+2D(g) ΔH<0;达到平衡(Ⅰ)时,V(乙)="0.86V" L。请回答:
C(g)+2D(g) ΔH<0;达到平衡(Ⅰ)时,V(乙)="0.86V" L。请回答: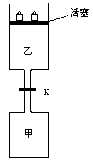
(1)乙中B的转化率为
(2)甲中D和乙中C的物质的量比较:(填“相等”、“前者大”、“后者大”);
(3)打开K,过一段时间重新达平衡(Ⅱ)时,乙的体积为(用含V的代数式表示,连通管中气体体积忽略不计。)