(10菏泽15)、用“侯氏制碱法”制得的纯碱常含有少量的氯化钠(假定只含氯化钠杂质)。称量某纯碱样品12g,全部溶解在100g水中,所得溶液与160g氯化钙溶液混合,恰好完全反应。过滤干燥后,称得沉淀质量为10g。请计算:
(1)纯碱样品中碳酸钠的质量分数。
(2)反应后所得滤液中溶质的质量分数。
右图是两种化肥标签的一部分,请回答:
(1)从标签上看,两种化肥具有共同的物理性质之一是;碳酸氢铵不同于尿素的化学性质是。
(2)尿素的相对分子质量为
(3)从含氮量角度,50kg这种碳酸氢铵相当于kg(精确到0.1)这种尿素。
小明同学为测定某稀硫酸溶液浓度(即溶质质量分数),他取该稀硫酸溶液20 g,将30g氢氧化钡溶液分三次加入该稀硫酸溶液中,测得三次反应的有关数据见下表:
| 第一次 |
第二次 |
第三次 |
|
| 加入氢氧化钡溶液的质量/g |
10 |
10 |
10 |
| 生成沉淀的质量/g |
0.923 |
1.864 |
2.33 |
请根据有关数据进行分析与计算:
(1)20g该稀硫酸溶液与氢氧化钡溶液完全反应时生成沉淀的质量为g。
(2)将第三次反应后所得的混合液过滤,得到滤液的质量为g。
(3)该稀硫酸溶液的浓度(即溶质质量分数)为多少?(写出计算过程)
(4)小明同时用pH计测定并记录该稀硫酸溶液与氢氧化钡溶液反应过程中混合溶液pH变化情况(如下图所示),请你用虚线在图中标出该稀硫酸溶液与氢氧化钡溶液刚好完全反应时的变化点,并注明pH和所反应的氢氧化钡溶液的质量。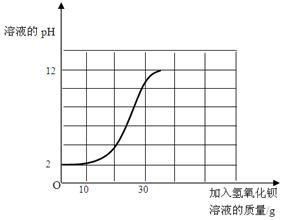
人体缺乏维生素C(简写“Vc”)会患坏血病。下图所示为某种“维生素C”说明书的一部分,请回答: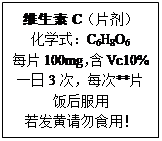
(1)“Vc”中C、H、O三种元素的质量比是_____________。
(2)若正常成人每天对“Vc”的最低需要量为60mg:
①当这些“Vc”完全来自右图的“维生素C”时,则每次服用“维生素C”至少_______片。
②当这些“Vc”完全来自某种新鲜蔬菜(每1000g这种蔬菜含“Vc” 120mg)时,每天至少应食用这种蔬菜___________g。
甲、乙、丙三位同学对氯化镁固体样品(仅含杂质NaCl)进行如下检测:各取5.0g样品(样品中MgCl2、NaCl均匀分布)溶于一定量的水中得到25.0g溶液,再加入不同质量,溶质质量分数为10%的氢氧化钠溶液,反应得到沉淀的质量如下表:
| 甲 |
乙 |
丙 |
|
| 加入NaOH溶液的质量(g) |
35.0 |
40.0 |
45.0 |
| 反应得到沉淀的质量(g) |
2.5 |
2.9 |
2.9 |
请回答下列问题:
(1)上述实验中,____________同学所用的氢氧化钠溶液一定过量。
(2)计算乙同学实验后所得溶液(NaCl)溶质质量分数(结果精确到0.1%)。
(11分)某化学兴趣小组为了测定某稀硫酸的溶质质量分数,取100g稀硫酸于烧杯中,向烧杯中逐滴滴入质量分数为10%的的氢氧化钠溶液,反应过程中所得溶液的酸碱度变化如右图: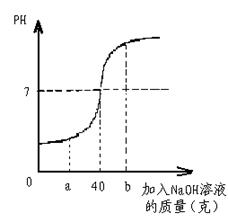
(1)当加入氢氧化钠溶液的质量为a g时,所得溶液中的溶质是__________(填化学式);
当加入氢氧化钠溶液的质量为b g时,向所得溶液中滴加酚酞溶液,溶液呈色。
(2)稀硫酸的溶质质量分数是?
(3)如果将NaOH溶液换成10%的KOH溶液,当所得溶液的PH="7" 时,所加KOH溶液的质
量40g(填“<”或“>”或“=”)。