(10梧州50).现有硫酸和硫酸铜的混合溶液200 g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液直至生成Cu(OH)2沉淀,沉淀质量与所加入的氢氧化钠溶液的质量关系如图20所示。求:
(1)Cu(OH)2的相对分子质量是 。
(2)生成最大沉淀量时所加入的氢氧化钠溶液的总质量。
某钢铁厂每天需消耗1000t含氧化铁80%的赤铁矿石,该厂理论上可以炼出含铁96%的生铁的质量是多少?
目前全世界的燃煤工厂和发电厂都应用湿净化器对煤燃烧后产生的烟气脱硫,主要反应原理为: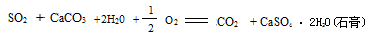
某工厂现有12.5t含杂质20﹪的石灰石(杂质不参加反应),最多可以吸收SO2多少吨
煅烧石灰石可制得生石灰,如果要制取2.8t氧化钙,需要碳酸钙的质量是多少?
将Na2CO3和NaCl固体混合物22.3 g放入烧杯中,加入182.1 g稀盐酸恰好完全反应。待没有气泡逸出后,称量烧杯中剩余物质总质量为200 g。请计算:
(1)生成二氧化碳的质量是___;
(2)所得溶液中溶质的质量分数是多少?
某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如下图所示。
求:(1)计算碳酸钠中各元素的质量比:Na:C:O=。
(2)碳酸钠的相对分子质量为:。
(3)生成CO2的质量。
(4)该纯碱样品中Na2CO3的质量分数。