下列说法正确的是
| A.常温下,PH=7的CH3COONa和CH3COOH的混合溶液[c(Na+)=0.1mol/L]中各离子浓度关系:c(CH3COOH)>c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
| B.0.1mol/LNa2CO3溶液中:c(Na+)>c(CO32-)> c(HCO3-)>c(OH-) |
| C.0.1mol/LNaHCO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
| D.向0.2 mol/LNaHCO3溶液中加入等体积的0.1mol/LNaOH溶液:c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是()
4NO(g)+6H2O(g),下列叙述正确的是()
| A.化学反应速率关系是:2v正(NH3)=3v正(H2O) |
| B.若单位时间内生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态 |
| C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 |
| D.达到化学平衡时,4v正(O2)=5v逆(NO) |
已知反应:①2Na(s)+1/2O2(g)=Na2O(s) △H1=-414kJ/mol ②2Na(s)+O2(g)=Na2O2(s) △H2=-511kJ/mol
下列说法正确的是 ( )
| A.①和②产物的阴阳离子个数比不相等 |
| B.①和②生成等物质的量的产物时,转移电子数不同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.反应:Na2O2(s)+2 Na(s)= 2Na2O(s) △H=-317kJ/mol |
右图是某条件下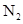 与
与 反应过程中能量变化的曲线图。根据图像判断下列叙述中正确的是()
反应过程中能量变化的曲线图。根据图像判断下列叙述中正确的是()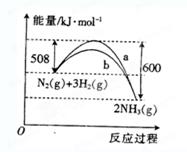
A.该反应的热化学方程式为 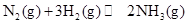 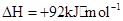 |
B.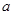 曲线是加入催化剂时的能量变化曲线 曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热数值会减小 |
D.反应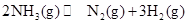 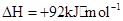 |
与实际化工生产流程相符的叙述是( )
| A.制备硝酸的工业中,理论上氨中的氮元素100%转化为了硝酸 |
| B.制备硫酸的工业尾气用氢氧化钠溶液吸收 |
| C.让Cl2在H2中燃烧制氯化氢,将氯化氢气体通入水中获得盐酸 |
| D.工业上用电解熔融氧化铝和冰晶石的混合物的方法得到铝 |
“绿色化学”是当今社会提出的一个新概念.在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得产物,即原子的利用率为100%.在用丙炔合成甲基丙烯酸甲酯 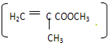 的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是( )
的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是( )
| A.CO和CH3OH | B.CO2和H2O | C.CH2=CH2和CO | D.CH3OH和H2 |