已知丙二酸二乙酯能发生以下反应:
有机物A在一定条件下可以发生如下图所示的转化(其他产物和水已省略)。其中相关物质的结构和性质为:A不含甲基,能与金属钠反应生成氢气;B所含碳原子数与A相同,且只含有一种官能团;C能发生银镜反应;1molD与足量碳酸氢钠溶液反应可产生二氧化碳2mol。
请结合图中其它信息回答下列问题:
(1)写出下列物质所具有的官能团的名称:C___________,D___________
(2)①~⑤反应中,属于取代反应的是________________(填序号)。
(3)写出A、G的结构简式:A__________ _, G_______ __________
(4)写出②、④反应的化学方程式:
②________________________________________________________________。
④_________________________________________________________________。
(1)在25℃条件下将pH=10的氨水稀释10倍后溶液的pH为(填序号)________。
A.9 B.11 C.9~10之间 D.9~11之间
(2)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,溶液pH_________(填“增大”、“减小”或“不变”),主要原因是________________。
(3)已知某溶液中只存在NH4+、H+、OH-、Cl-四种离子,该溶液中各离子浓度大小顺序可能有如下几种关系:
A.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-)
①上述离子浓度大小关系不可能的是_________(填序号)。
②若溶液中只溶解了一种溶质,则该溶质是____________,上述离子浓度大小顺序关系中正确的是(选填序号)________________。
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl) ________ c(NH3·H2O)(填>、<或=)
(4)25℃时,如果将0.1molNH4Cl和0.05molNaOH溶于水,形成混合溶液,(假设无气体逸出损失),则NH4+和NH3·H2O两种粒子的物质的量之和等于________mol。
在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g)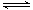 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应为_________反应(选填“吸热”、“放热”)。
(2)能判断该反应是否达到化学平衡状态的依据是______________。
a.容器中压强不变b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_______℃。
(4)1200℃时,某体系中CO2、H2、CO、H2O的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时上述反应的方向为____________。(选填“正向”“逆向”或“不移动”)。
2SO2(g)+O2(g) 2SO3(g) △H=-198kJ/mol,反应过程的能量变化如图所示。
2SO3(g) △H=-198kJ/mol,反应过程的能量变化如图所示。
请回答下列问题:
(1)图中A表示__________,该反应加入V2O5作催化剂后E如何变化_______(填“升高”、“降低”或“不变”)。
(2)如果反应速率v(SO2)为0.05mol/(L·min),则v(O2)="_________" mol/(L·min)、v(SO3)=_____mol/(L·min)
(3)已知单质硫燃烧热的数值为296kJ/mol,则1molS(s)完全反应生成SO3(g)时放出的热量为________kJ。
(4)某人设想以如图所示装置用电化学原理生产硫酸,通入O2的一极为_______________(填写“正”或“负”)极;写出通入SO2一极的电极反应____________________。
下图为教材中测定中和热的简易量热计。
(1)图中尚缺少的玻璃仪器是_____________,实验中若用金属质地的仪器来代替会使得的△H___(填“偏高”、“偏低”或“无影响”)。
(2)如果用50mL0.50mol/L的盐酸和50mL0.55mol/L的氢氧化钠溶液进行实验,已知二者的密度均为1g/cm3,比热容c=4.18J/(g·℃),实验起始温度为t1℃,终止温度为t2℃,则中和热△H为______kJ/mol,实验中氢氧化钠溶液比盐酸浓度大的原因是____________________。
(1)13.2g氮的氧化物(NxO)中氧原子物质的量为0.3mol,该质量的NxO在标况下的体积为__________L,x的值为_________。
(2)化合物A的分子组成可用NxHy表示,在一定条件下可发生分解反应,15mLA气体完全分解生成5mL N2和20mL NH3(同温、同压)。A的化学式为_________________。
(3)20mL Al2(SO4)3溶液加水稀释至100mL,稀释后的溶液中SO42-的物质的量浓度为0.3mol∙L-1。则稀释前Al2(SO4)3的物质的量浓度为________________。