以节能减排为基础的低碳经济是保持社会可持续发展的战略举措。下列做法违背发展低碳经济要求的是
| A.发展氢能和太阳能 | B.举行“地球一小时”熄灯活动 |
| C.限制塑料制品的使用 | D.种植农作物时大量使用化肥和农药 |
下列各组离子在指定溶液中能大量共存的是
| A.滴入甲基橙显红色的溶液中:K+、Al3+、I-、ClO-、NO3- |
| B.常温下,某溶液pH=1的溶液中含有:NO3-、NH4+、Fe2+、SO42- |
| C.常温下,c(H+)/c(OH-)=1×10-12的溶液:K+、AlO2-、CO32-、Na+ |
| D.0.1mol/LFeCl3溶液中:Fe2+、NH4+、SCN-、SO42- |
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是
| X |
Y |
Z |
|
| ① |
NaOH溶液 |
SiO2 |
氢氟酸 |
| ② |
O2 |
N2 |
H2 |
| ③ |
双氧水 |
SO2 |
BaCl2溶液 |
| ④ |
FeCl3溶液 |
Cu |
浓硝酸 |
A.①③ B.①④C.②④D.②③
下列物质的转化在给定条件下能实现的是
| A.①④ | B.②③ | C.②③④ | D.①③④ |
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是
①向饱和碳酸钠溶液中通入过量CO2②向NaAlO2溶液中逐滴加入过量的稀盐酸
③向AlCl3溶液中逐滴加入过量稀NaOH溶液④向硅酸钠溶液中逐滴加入过量的盐酸
⑤向AgNO3溶液中逐滴加入稀氨水
| A.①② | B.②③ | C.①④ | D.④⑤ |
NaCl是一种重要的化工原料,如图所示,可以制备系列物质。下列说法正确的是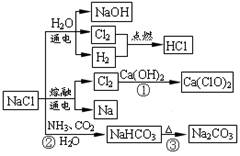
| A.反应②③是侯氏制碱法的原理 |
| B.反应①中的Ca(ClO)2是还原产物 |
| C.常温下干燥Cl2可储存于钢瓶中,所以Cl2与铁不反应 |
| D.图中所示转化反应都是氧化还原反应 |