锂元素(元素符号为Li)及其所形成的化合物,在通讯和航空航天领域中具有极其重要的用途。它的化合物氢氧化锂(LiOH)是一种易溶于水的白色固体,有辣味,具有强碱性和腐蚀性。
(1)写出氢氧化锂的一条物理性质________________________________;
(2)右表是部分物质的溶解性表,运用此溶解性表并结合你对复分解反应发生条件的理解,从表中选出一种盐,该盐能和LiOH发生复分解反应,请你写出该盐的化学式:_____________________________________________。
| |
OH- |
CO32- |
SO42- |
NO3- |
| Ba2+ |
溶 |
不 |
不 |
溶 |
| Cu2+ |
不 |
不 |
溶 |
溶 |
| Li+ |
溶 |
微溶 |
溶 |
溶 |
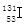 原子是常规核裂变的产物之一,可以通过测定空气或水中
原子是常规核裂变的产物之一,可以通过测定空气或水中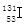 的含量监测和电站是否发生泄漏。
的含量监测和电站是否发生泄漏。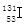 原子核内有53个质子和78个中子。下列说法中,错误的是
原子核内有53个质子和78个中子。下列说法中,错误的是
| A.其原子核外有53个电子 | B.其相对原子质量约为131 |
C.与 原子属于同一种元素 原子属于同一种元素 |
D.其核电荷数为78 |
次氯酸钠(NaClO)是某种家用消毒液的主要成分,其中氯元素的化合价为
| A.+1 | B.-1 | C.+3 | D.+5 |
适量补充矿物质对人体健康非常重要。下列有关说法错误的是
| A.缺铁会引发贫血 | B.儿童缺锌会发育迟缓 |
| C.老年人缺钙会患骨质疏松 | D.儿童缺钙会导致智力低下 |
下列物质,属于氧化物的是
| A.HNO3 | B.O2 | C.CaO2 | D.MgCl2 |
下列物质的用途,主要由物理性质决定的是
| A.氢气做火箭的燃料 | B.浓硫酸做干燥剂 |
| C.二氧化碳做温室肥料 | D.盐酸用于除铁锈 |