某同学用下列装置制备并检验Cl2的性质。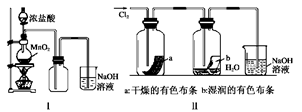
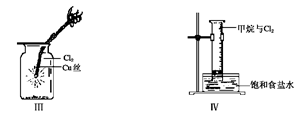
下列说法正确的是( )
| A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗 |
| B.Ⅱ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
| C.Ⅲ图中:生成蓝色的烟 |
| D.Ⅳ图中:量筒中发生了加成反应 |
下列有关化学用语表示正确的是
| A.丙烯的结构简式:C3H6 |
| B.氢氧根离子的电子式:[····H]- |
C.氯原子的结构示意图: |
| D.中子数为146、质子数为92的铀(U)原子:92 U |
下列有关化学用语或名称,表达错误的是
A.COCl2分子的结构式: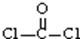 |
B.苯分子的比例模型: |
| C.铁在潮湿的空气中腐蚀,负极的电极反应式:Fe-2e-===Fe2+ |
D.溴化铵的电子式: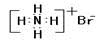 |
下列逻辑关系图示中正确的是
下列化学用语使用不正确的是
A.Na+的结构示意图为 |
| B.明矾的化学式为KAl(SO4)2·12H2O |
| C.聚乙烯的结构简式为CH2==CH2 |
| D.高氯酸(HClO4)中氯元素的化合价为+7 |
下列有关分类的观点正确的是
①由苯制取溴苯、硝基苯、环己烷的反应都属于取代反应
②铅蓄电池、锂电池、碱性锌锰电池都属于二次电池
③碳素钢、不锈钢和目前流通的硬币都属于合金
④生物质能、沼气和乙醇都是可再生能源
⑤氨水、醋酸、氢氧化铝都属于弱电解质
| A.①② | B.②④ | C.③④ | D.③⑤ |