下列化学用语表达正确的是 ( )
A.氯化钠的电子式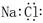 : : |
B.丙烷分子的比例模型: |
| C.NaHCO3的电离方程式NaHCO3=Na++H++CO32- |
| D.质子数为53,中子数为78的碘原子:131 53I |
下列有关铝的说法正确的是
| A.金属铝与盐酸或氢氧化钠溶液分别反应均产生0.2 mol氢气时,失去的电子数不同 |
| B.铝既能与盐酸反应(生成AlCl3),又能与NaOH溶液反应(生成NaAlO2),所以金属铝具有两性 |
| C.金属铝能在空气中形成一层致密的氧化膜,因此是一种比较活泼的金属,所以将少量铝投入到过量的FeCl3溶液中,可以置换出金属铁 |
| D.铝元素在人体内聚集过多,对健康不利,建议尽量少用铝制餐具、铝制食品包装袋、铝制易拉罐等 |
下列各组括号内的试剂,不能用于除掉各物质中的杂质的是
| A.铁粉中混有锌粉杂质(稀硫酸) |
| B.FeCl3中混有FeCl2杂质(Cl2) |
| C.CO气体中混有CO2杂质(NaOH溶液) |
| D.SiO2中混有CaCO3杂质(盐酸) |
钛和钛合金是21世纪的重要金属材料。它们具有优良的性能,如熔点高、密度小、可塑性好、机械性能好、抗腐蚀能力强,钛合金与人体有很好的“相容性”。根据它们的主要性能,不合实际的用途是
| A.用于核潜艇设备的制造 |
| B.用于制造航天设备 |
| C.用来作保险丝 |
| D.可用来制造人造骨 |
下列说法正确的是()
| A.常温常压下,只有一种元素的单质呈液态 |
| B.周期表中所有元素都是从自然界中发现的 |
| C.过渡元素不全是金属元素 |
| D.常温常压下,气态单质的分子都是由非金属元素的原子形成的 |
X、Y是元素周期表第ⅦA族中的两种元素。下列叙述中能说明X的非金属性比Y强的是()
| A.X原子的电子层数比Y原子的电子层数多 |
| B.X的氢化物的沸点比Y的氢化物的沸点低 |
| C.X的气态氢化物比Y的气态氢化物稳定 |
| D.Y的单质能将X从NaX溶液中置换出来 |