某次硫酸铜晶体结晶水含量的测定实验中,相对误差为-2.67%,其原因可能是( )
| A.实验时盛放硫酸铜晶体的容器未完全干燥 |
| B.加热过程中晶体有少量溅失 |
| C.硫酸铜晶体中含有不分解失重的杂质 |
| D.加热后固体未放入干燥器中冷却 |
在1200℃时,天然气脱硫工艺中会发生下列反应
H2S(g)+ 3/2O2(g)=SO2(g)+H2O(g) △H1
2H2S(g)+SO2(g)=3/2S2(g)+2H2O(g) △H2
H2S(g)+1/2O2(g)=S(g)+H2O(g) △H3 2S(g) =S2(g) △H4
则△H4的正确表达式为
| A.△H4=2/3(△H1+△H2-3△H3) | B.△H4=2/3(3△H3-△H1-△H2) |
| C.△H4=3/2(△H1+△H2-3△H3) | D.△H4= 3/2(△H1-△H2-3△H3) |
反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率V(x)可表示为
| A.V(NH3)=0.010mol/(L·S) | B.V(O2)=0.0010mol/(L·S) |
| C.V(NO)=0.0010mol/(L·S) | D.V(H2O)=0.045mol/(L·S) |
一定条件下,充分燃烧一定量的丁烷放出热量161.9 kJ,经测定完全吸收生成的二氧化碳需消耗5mol/L的KOH溶液100mL,恰好生成正盐。则此条件下热化学方程式: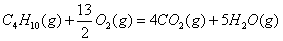 的ΔH为
的ΔH为
| A.+2590.4KJ/mol | B.-2590.4KJ/mol |
| C.+1295.2KJ/mol | D.-1295.2KJ/mol |
已知:2Zn(s) + O2(g)= 2ZnO(s) △H1= -701.0kJ·mol-1,2Hg(l)+ O2(g)= 2HgO(s) △H2= -181.6kJ·mol-1,则反应Zn(s) + HgO(s)= ZnO(s) + Hg(l)的△H为:
| A.+519.4 kJ·mol-1 | B.+259.7 kJ·mol-1 |
| C.-259.7 kJ·mol-1 | D.-519.4 kJ·mol-1 |
已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H—O键形成时放出热量463 kJ,则氢气中1 mol H—H键断裂时吸收热量为
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |