NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
| A.5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA |
| B.常温常压下,1mol氦气含有的核外电子数为4NA |
| C.7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA |
| D.0.5mol雄黄(As4S4,结构如图)含有NA个S—S键 |
己知丙烷的燃烧热△ =-2215 ,若一定量的丙烷完全燃烧后生成1.8 水,则放出的热量约为()
| A. | 55 | B. | 220 | C. | 550 | D. | 1108 |
0.1 下列气体分别与1 0.l 的 溶液反应,形成的溶液 最小的是()
| A. | B. | C. | D. |
下列离子中半径最大的是()
| A. | B. | C. | D. |
化学与生活密切相关。下列应用中利用了物质氧化性的是()
| A. | 明矾净化水 | B. | 纯碱去油污 |
| C. | 食醋除水垢 | D. | 漂白粉漂白织物 |
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32−、SO42−、NO3−中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如下图所示。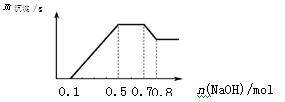
则下列说法正确的是
| A.溶液中的阳离子只有H+、Mg2+、Al3+ |
| B.溶液中一定不含CO32−,可能含有SO42−和NO3− |
| C.溶液中n(NH4+)=0.2mol |
| D.n(H+)∶n(Al3+)∶n(Mg2+) = 1∶1∶1 |