以色列科学家达尼埃尔·谢赫特曼因发现“准晶体”而独享2011年诺贝尔化学奖。1982年谢赫特曼首次观察到一种“准晶体”现象,“准晶体”原子结构打破了传统晶体内原子结构必须具有重复性这一黄金法则,在当时引起极大争议,并被迫离开当时的研究小组。但随后,科学家们在实验室中制造出了越来越多的各种准晶体,并于2009年首次发现了纯天然准晶体。下列认识错误的是
| A.科学家开创性的发现是决定科学发展的唯一途径 |
| B.实验是科学发现的重要手段,科学发现往往需要建立在实验事实的基础之上 |
| C.人类对物质结构的探索是无止境的,对物质世界的认识也是不断深入的 |
| D.最伟大的科学家也会陷于传统藩篱的桎梏中,保持开放的头脑、敢于质疑现有认知是科学家最重要的品质 |
有关SO2说法错误的是
| A.单质硫在空气中燃烧可生成SO2 |
| B.SO2能使品红溶液褪色是因为它具漂白性,加热可恢复原本红色 |
| C.SO2和Cl2都具有漂白作用,所以将两种气体等物质的量同时作用于潮湿有色物,可增强漂白作用 |
| D.SO2能使加酚酞的NaOH溶液褪色是因为它能与NaOH反应 |
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
下列有关说法正确的是
| A.过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.步骤④的作用是达到富集溴的目的 |
| C.过程②中MgCl2·6H2O加热脱水制得无水MgCl2 |
| D.工业上电解熔融精盐的过程称为氯碱工业 |
某恒温密闭容器中,可逆反应A(s) B+C(g) ΔH=" +Q" kJ·mol-1(Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
B+C(g) ΔH=" +Q" kJ·mol-1(Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
A.产物B的状态只能为固态或液态
B.平衡时,v(A)消耗﹕n(C)消耗=1﹕1
C.保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
D.若开始时向容器中加入1molB和1molC,达到平衡时放出热量Q kJ
现有短周期主族元素X、Y、Z、R、T。R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡。六种元素的原子半径与原子序数的关系如图所示。下列推断正确的是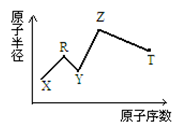
| A.原子半径和离子半径均满足:Y < Z |
| B.氢化物的沸点排序 :Y > T > R |
| C.最高价氧化物对应的水化物的酸性 :T < R |
| D.由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性 |
在55℃时,下列说法正确的是
| A.向水中加入少量硫酸氢钠固体,促进了水的电离,c(H+)增大,Kw不变 |
| B.pH=8的NaHCO3溶液中:c(OH-)=1×10-6mol/L |
| C.饱和氯水中: c(Cl-)=c(ClO-)+c(HClO) |
| D.0.1mol/L的(NH4)2SO4溶液中:c(SO42-)> c(NH4+) > c(H+) > c(OH-) |