已知:N2(g)+3H2(g) 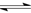 2NH3(g) △H =-92.4 kJ·mol-1,在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
2NH3(g) △H =-92.4 kJ·mol-1,在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 |
容器1 |
容器2 |
| 反应物投入量始态 |
1mol N2、3mol H2 |
2mol NH3 |
| NH3的平衡浓度/mol·L-1 |
cl |
c2 |
| 反应的能量变化 |
放出a kJ |
吸收b kJ |
| 体系压强/Pa |
p1 |
p2 |
| 反应物转化率 |
α1 |
α2 |
下列说法不正确的是 ( )
A. cl 一定等于c2 B.a + b = 92.4
C. p1 一定等于p2 D.α1 一定等于α2
下列各组物质的分类正确的是
| A.同位素:1H+、2H2、3H |
| B.同系物:丙烷、异丁烷、新戊烷 |
| C.电解质: 冰醋酸、水银、烧碱 |
| D.酸性氧化物:一氧化氮﹑二氧化碳、三氧化硫 |
将1.95g锌粉加入到200mL的0.100 mol·L-1MO2+溶液中,恰好完全反应,则还原产物可能是()
| A.M | B.M2+ | C.M3+ | D.MO2+ |
下列实验设计或实验操作中,正确的是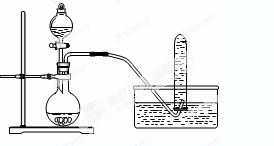
| A.铜与浓硝酸反应制NO2:可采用下图装置 |
| B.分离乙酸和乙醇溶液:用分液漏斗进行分离 |
| C.稀硫酸和锌粒反应制取氢气:加入少许硫酸铜以加快反应速率 |
| D.鉴别Na2CO3溶液和NaHCO3溶液:分别向两种溶液滴加澄清石灰水至过量 |
下图装置(Ⅰ)是一种可充电电池,装置(Ⅱ)为电解池。
装置(Ⅰ)的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为2Na2S2+NaBr3化气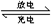 Na2S4+3NaBr。当闭合开关K时,X电极附近溶液变红。下列说法正确的是
Na2S4+3NaBr。当闭合开关K时,X电极附近溶液变红。下列说法正确的是
| A.闭合开关K时,钠离子从右到左通过离子交换膜 |
| B.闭合开关K时,负极反应式为:3NaBr-2e-=NaBr3+2Na+ |
| C.闭合开关K时,X电极反应式为:2Cl--2e-=Cl2↑ |
| D.闭合开关K时,当有0.1molNa+通过离子交换膜,X电极上析出标准状况下气体1.12L |
下列仪器中具有①溶解固体,②配制溶液,③加热较多量液体三种用途的是()
| A.集气瓶 | B.量筒 |
| C.试管 | D.烧杯 |