我们的日常生活离不开金属。
⑴右图是金属的一个应用实例,请说出利用了金属的什么物理性质? (答出一点即可) 。
(2)据有关资料报导,现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%—40%。铁生锈是铁与空气中的水蒸气、_ 等发生化学反应的过程。
(3)在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)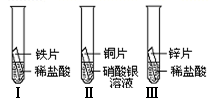
①一段时间后,可观察到实验Ⅱ的现象是 ;
反应的化学方程式是
②小组中的甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁的金属活动性强弱。你认为他依据的实验现象是 。
③乙和丙两位同学认为上述三个实验不能够得出四种金属的活动性顺序,原因是 ;并在上述实验的基础上,补充了一个实验(右图所示),实现了探究目的。他们的实验:X是金属______,Y是__________溶液(写出化学式)。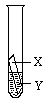
(5分)请根据图中a、b、c三种物质的溶解度曲线,回答下列问题: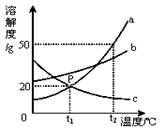
(1)P点的含义是.
(2)t2℃时,将30g的a物质加入到50 g水中不断搅拌,能形成g溶液.
(3)如何通过改变温度的方法将接近饱和的c溶液变成饱和溶液?
(4)将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,溶液中溶质质量分数由大到小的顺序是.
(5)b中混有少量a,可采用将b提纯.(填“降温结晶”或“蒸发结晶”)
(12分)化学来源于生活,服务于生活.请回答下列生活中的有关化学问题.
(1)用符合要求的字母填空
a.稀盐酸
b.氯化钠
c.氢氧化钠
d.碳酸氢钠
e.硫酸铜
①可用于治疗胃酸过多的是
②可用于游泳池消毒的是
③可用于金属表面除锈的是
④厨房里常见的调味品是
(2)天然气或沼气已在城乡普遍入户,请写出天然气燃烧的化学方程式
(3)节假日双休日,去野炊实为一大快事.
①野炊所带的如下物品中,由有机合成材料制成的是(填字母);
A.纯棉毛巾 B.玻璃杯 C.塑料袋 D.铁锅
②野餐食谱如下:主食:馒头
配菜:红烧肉、豆腐汤、牛肉干,从营养角度来看,你认为食谱还应添加(填字母) ;
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
③同学们用洗涤剂除去油污,是利用了洗涤剂的作用;
④野炊后同学们留下了一堆垃圾,他们准备分类堆放.其中不可放入可回收垃圾箱中的是_____(填字母).
A.废纸 B.果皮 C.易拉罐 D.塑料桶
(4)漂白粉可用于自来水的杀菌、消毒,它的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙可发生如下反应:Ca(ClO)2+ X + H2O= CaCO3↓+ 2 HClO,则x的化学式为
(5)NH4Cl是常用的氮肥,但施用时不能和熟石灰混合施用,请用方程式解释原因___________
(6)雾霾是一种灾害性天气现象,由于人类生产、生活向大气中排放大量细颗粒物,如果通过大气的自净能力,又遇到静稳天气,就会出现雾霾现象.请分析下列污染物中,会导致雾霾的是(填字母)
A.二氧化硫 B.氢氧化物 C.一氧化碳 D.PM2.5
在宏观、微观和符号之间建立联系是化学学科的特点。
(1)硫酸铜、汞、氢气三种物质中,由原子构成的是(写化学式)。
(2)下图表示核电荷数为11~17的元素最高和最低化合价。
①硫元素的最高正价氧化物的化学式为。
②若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为。
(3)在点燃条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如下所示。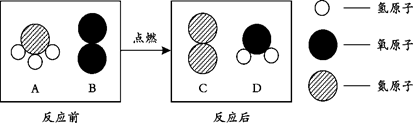
①该反应的基本反应类型为。
②该反应中A、C两种物质的质量比为。
(4)下图表示氢氧化钠溶液与稀盐酸反应的微观过程。
请你在下图圆圈中处将BaCl2溶液和CuSO4溶液反应的产物补充完整:
2015年世界水日的主题是“水与持续发展”。
Ⅰ.水的组成:
(1)用下图装置通电一段时间后,b中所收集气体的为,化学方程式为。
(2)下列还能确认水是由氧元素和氢元素组成的实验是(填序号)。
| A.氢气在氧气中燃烧 | B.水的蒸发 |
| C.氢气还原氧化铜 | D.氢气在氯气中燃烧 |
Ⅱ.水的净化:
小丹同学收集到一瓶浑浊的河水,利用如下流程来净化水,最终制成蒸馏水。
回答下列问题:
(1)若要测定该河水的酸碱度常用。
(2)A加入的物质是明矾,操作①需要用到的三种玻璃仪器是烧杯、玻璃棒、。
(3)操作②中选用除去水中色素和异味。
(4)小丹同学取少量液体D于试管中,加入少量,振荡,发现有少量泡沫且有浮渣产生,说明液体D是硬水。
(5)上述净化水的单一操作中,净化程度最高的是(填“操作①”、“操作②”或“操作③”)
Ⅲ.水的作用:
下图实验中水的作用分别是:
甲:;乙:。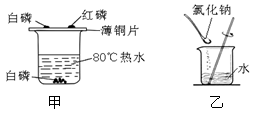
汽车、电动车一般使用铅酸蓄电池。某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸。
(1)若用50 g质量分数为98%的浓硫酸配制该稀硫酸时,用量筒量取水mL(水的密度可看作为1 g/cm3)。
(2)在实验室用浓硫酸配制稀硫酸的主要步骤有:计算、量取、、装瓶并贴上标签。
(3)为了实验的安全,在稀释时应将沿容器壁慢慢倒入中,并用玻璃棒不断搅拌。若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后再涂上3%~5%的溶液。
(4)用配制的硫酸溶液与氢氧化钠溶液反应,实验过程中溶液的pH变化曲线如图所示:A点对应的溶液
呈(填“酸性”、“碱性”或“中性”);C点对应的溶液中的溶质为(写化学式)。