铝不易被腐蚀,其主要原因是因为铝
| A.是一种轻金属 | B.金属活动性比镁弱 |
| C.具有高熔点 | D.易形成致密的氧化物薄膜 |
下列说法正确的是
A.按系统命名法, 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 |
| B.常压下,正戊烷、异戊烷、新戊烷的沸点依次增大 |
C.肌醇 与葡萄糖 与葡萄糖 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 |
D.1.0 mol的 最多能与含5.0 mol 最多能与含5.0 mol |
NaOH的水溶液完全反应
下列有关化学用语表示正确的是
| A.乙酸的结构简式: C2H4O2 | B.F-的结构示意图: |
| C.中子数为20 的氯原子:2017Cl | D.NH3的电子式: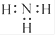 |
以下实验中能够获得成功的是
| A.以盐酸、石灰石、苯酚钠溶液为试剂,验证酸性强弱:盐酸>碳酸>苯酚 |
| B.除去溴苯中的少量溴:加入KI溶液,充分反应后,弃去水溶液 |
| C.实验室只用乙醇和乙酸混合加热就可以制取乙酸乙酯 |
| D.检验溴乙烷中的溴元素:在溴乙烷中滴入氢氧化钾溶液,加热后用硫酸酸化,再滴加硝酸银 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.标况下,11.2L的戊烷含有分子数为0.5NA个 |
| B.常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 |
| C.1L浓度为1mol·L-1的Na2CO3溶液中含有NA个CO32- |
| D. 1L 1mol/L的盐酸溶液中,所含氯化氢分子数为NA |
胡椒酚(结构如下图所示)是植物挥发油中的一种成分。关于胡椒酚的下列说法:①该化合物属于芳香烃;②分子中至少有7个碳原子处于同一平面;③它的部分同分异构体能发生银镜反应;④1mol该化合物最多可与2molBr2发生反应。其中正确的是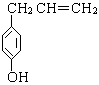
| A.①③ | B.①②④ | C.②③ | D.②③④ |