已知298K时,

 ,△H
,△H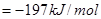 ,在相同温度下,向固定体积的密闭容器中通入
,在相同温度下,向固定体积的密闭容器中通入 和
和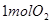 ,达到平衡时放出热量
,达到平衡时放出热量 ;向另一个同体积的密闭容器中通入
;向另一个同体积的密闭容器中通入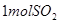 和
和 ,达到平衡时放出热量为
,达到平衡时放出热量为 ,则下列关系中正确的是
,则下列关系中正确的是
A. |
B. |
C. |
D.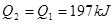 |
某有机物M的结构简式如图所示,下列叙述正确的是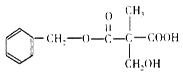
| A.其分子式为C12H12O5 |
| B.M中含有2种含氧官能团 |
| C.M能够发生加成、取代和加聚反应 |
| D.1 mol M和足量的NaOH溶液反应,可以消耗2 mol NaOH |
A可能为Na、C、Si、H2S中的一种或几种,可以实现下列转化关系的A有
A.1种 B.2种C.3种 D.4种
短周期元素X、Y、Z、W、Q在元素周期表中的位置如图所示,Z元素的简单离子半径在本周期中最小,下列说法不正确的是
| A.Y元素气态氢化物的稳定性大于X元素的气态氢化物 |
| B.形成的简单离子半径W>Q>Z>X |
| C.Q的最高价氧化物对应的水化物酸性最强 |
| D.X的最高价氧化物对应的水化物与其氢化物形成的化合物中含有离子键和共价键 |
化学与生活、环境密切相关,下列说法错误的是
| A.生活中钢铁制品生锈主要是由于吸氧腐蚀所致 |
| B.石油的裂化、裂解和煤的干馏都属于化学变化 |
| C.天然纤维、人造纤维、合成纤维组成元素相同 |
| D.工业废水中的Cu2+、Hg2+等重金属阳离子可以通过加入FeS除去 |
下列图示与对应的叙述相符的是: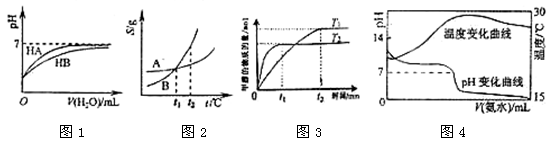
A.图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH。
B.图2表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B﹥A。
C.图3表示在其他条件相同时,分别在T1、T2温度下由CO2和H2合成甲醇的物质的量随时间变化情况,则CO2和H2合成甲醇是吸热反应。
D.图4表示将1.000 mol/L氨水滴入20.00mL1.000 mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线