下列表示溶液中所发生反应的离子方程式正确的是 ( )
A.NH4HCO3溶液与过量KOH浓溶液共热:NH4++ OH-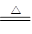 NH3↑+ H2O NH3↑+ H2O |
| B.Ca(HCO3)2溶液中加入少量NaOH溶液: Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O |
| C.KI溶液与H2SO4酸化的H2O2溶液混合: 2I-+ H2O2 + 2H+ =2H2O + I2 |
| D.向氯化银悬浊液中加入饱和碘化钾溶液:Ag+ +I-=AgI ↓ |
某有机物结构简式为: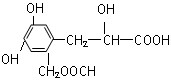 ,它可能发生的反应有:①加成反应;
,它可能发生的反应有:①加成反应;
②取代反应;③缩聚反应;④水解反应;⑤中和反应;⑥显色反应;⑦氧化反应;⑧还原反应;⑨消去反应;其中正确的是()
| A.③⑤⑥⑦ | B.全部 | C.④⑤⑥⑦ | D.除①④外其余都有 |
合成结构简式 的高聚物,其单体应是()
的高聚物,其单体应是()
①苯乙烯②丁烯③1,3—丁二烯④丙炔⑤苯丙烯
| A.①② | B.①③ | C.④⑤ | D.②④ |
分子式为C5H10O2的酯共有()(不考虑立体异构)
| A.9种 | B.10种 | C.8种 | D.7种 |
北京奥运会期间对大量盆栽鲜花施用了S—诱抗素制剂,以保持鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子的说法中正确的是()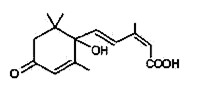
| A.含有碳碳双键、羟基、羰基、羧基 |
| B.含有苯环、羟基、羰基、羧基 |
| C.1mol该分子能与含2mol NaOH的溶液完全反应 |
| D.该分子能与溴水反应而使溴水褪色且1mol它能与溴水中的4 mol Br2反应 |
下列措施有利于节能减排,改善环境质量的有()
①在大亚湾核电站已安全运行多年的基础上,广东将继续发展核电,以减少火力发电带来的二氧化硫和二氧化碳排放问题
②积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料
③加速建设地铁、轻轨等轨道交通,促进珠三角城市一体化发展,减少汽车尾气排放
④发展低碳经济、循环经济,推广可利用太阳能、风能的城市照明系统
⑤使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾
| A.①②③④ | B.①②⑤ | C.①②④⑤ | D.③④⑤ |