“绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验。实验操作:钠与氯气反应的装置可作如图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成小球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是( )
| A.反应生成的大量白烟是氯化钠晶体 |
| B.钠着火燃烧产生苍白色火焰 |
| C.浸有NaOH溶液的棉球用于吸收未反应的氯气,以免污染空气 |
| D.用湿润的淀粉碘化钾试纸可以检验氯气是否被完全吸收 |
下列实验中操作、现象、结论对应关系正确的一组是()
| 选项 |
操作 |
现象 |
结论 |
| A |
在蔗糖中加入几滴水搅拌均匀,再加入浓硫酸,迅速搅拌 |
蔗糖逐渐变黑,体积膨胀,形成疏松多孔的物质 |
只体现了浓硫酸的脱水性 |
| B |
淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液 |
产生红色沉淀 |
淀粉水解可生成葡萄糖 |
| C |
溴乙烷和氢氧化钠溶液充分反应后,用足量稀硝酸酸化,再加入硝酸银溶液 |
生成淡黄色沉淀 |
溴乙烷中含有溴元素 |
| D |
将溴水加入苯中并充分振荡 |
溴水褪色 |
苯与溴发生了取代反应 |
以下四种有机物的分子式皆为C4H10O:
其中既能发生消去反应生成相应的烯烃,又能氧化生成相应醛的是()
| A.①② | B.只有② | C.②和③ | D.③和④ |
β紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。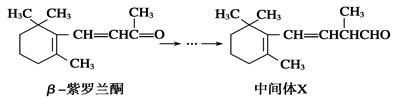
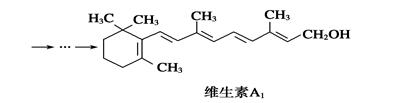
下列说法正确的是 ( )
| A.维生素A1易溶于NaOH溶液 |
| B.1 mol中间体X最多能与2 mol H2发生加成反应 |
| C.β紫罗兰酮可使酸性KMnO4溶液褪色 |
| D.β紫罗兰酮与中间体X互为同分异构体 |
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如下图所示: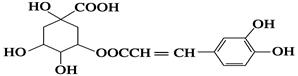
关于咖啡鞣酸的下列叙述正确的是 ( )
| A.分子式为C16H13O9 |
| B.1 mol咖啡鞣酸可与含8 mol NaOH的溶液反应 |
| C.能使酸性KMnO4溶液褪色,说明分子结构中含有碳碳双键 |
| D.与浓溴水能发生两种类型的反应 |
某化合物由碳、氢、氧三种元素组成,红外光谱图显示有三种共价键的振动吸收,核磁共振氢谱图显示有三个峰,峰面积比为6:1:1,则该有机物的结构简式是()
| A.C2H5OCH3 | B.CH3CH(OH)CH3 |
| C.CH3CH2CH2OH | D.CH3CH2CHO |