下列说法正确的是
| A.任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 |
| B.同温同压下,H2 (g)+Cl2(g)= 2HCl(g)在光照和点燃条件下的△H不同 |
| C.已知:①2H2(g) +O2(g) =2H2O(g) △H="–a" kJ·mol-1, ②2H2(g)+O2 (g)= 2H2O(1)△H="–b" kJ·mol-1,则a>b |
| D.已知:①C(s,石墨)+O2 (g)=CO2(g)△H=–393.5kJ·mol-1, |
②C(s,金刚石)+O2(g)=CO2 (g) △H="–395.0" kJ·mol-1,
则C(s,石墨)=C(s,金刚石)△H="+1.5" kJ.mol。1
同物质的量浓度的KCl、CaCl2、AlCl3三种溶液的体积比为3:2:1,这三种溶液中Cl﹣物质的量浓度之比是
| A.3:2:1 | B.1:2:3 | C.1:1:1 | D.2:3:1 |
容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的
| A.②④⑥ | B.③⑤⑥ | C.①②④ | D.①③⑤ |
为了探究FeSO4和Cu(NO3)2的混合物中各组分的含量,现设计如下流程。 下列叙述中错误的是
下列叙述中错误的是
| A.n = 0.02 |
| B.V = 2240 |
| C.原混合物中FeSO4的质量分数约为89% |
| D.m = 3.2 |
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化如图所示。已知W的一种核素的质量数为18,中子数为10;X是短周期元素中原子半径最大的;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是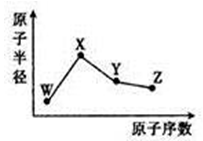
| A.简单离子半径:W>X>Z |
| B.最简单气态氢化物的稳定性:Y<Z |
| C.化合物XZW中既含离子键又含共价键 |
| D.Y的氧化物能与X的最高价氧化物对应的水化物反应 |
向一定量的盐酸中逐滴加入NaAlO2溶液,生成沉淀Al(OH)3的量随NaAlO2加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是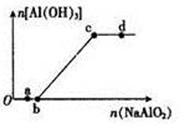
| A.a点对应的溶液中:Na+、Fe3+、SO42-、HCO3- |
| B.b点对应的溶液中:Ag+、Ca2+、NO3-、H+ |
| C.c点对应的溶液中:Na+、K+、SO42-、Cl- |
| D.d点对应的溶液中:K+、NH4+、I-、H+ |