将10g由Mg、Zn、Fe组成的混合物与40mL稀硫酸恰好完全反应,产生的氢气在标准状况下为5.6L,则三种金属的物质量之和为( )
| A.0.5mol | B.0.25mol | C.0.1mol | D.0.125mol |
某元素的原子结构示意图为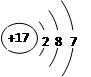 ,下列关于该原子的说法正确的是
,下列关于该原子的说法正确的是
| A.质子数为7 | B.最外层电子数为2 |
| C.核外电子数为7 | D.核外有3个电子层 |
下列物质属于单质的是
| A.石墨 | B.硫铁矿 | C.青铜 | D.碳素墨水 |
P2O5中P元素的化合价为
| A.+3 | B.+4 | C.+5 | D.+6 |
用mol•L—1作为单位的物理量是
| A.长度 | B.质量 | C.物质的量 | D.物质的量浓度 |
溴化碘(IBr)的化学性质与氯气相似,能跟大多数金属反应生成金属卤化物,能跟水反应:IBr+H2O=HBr+HIO,下列有关叙述中不正确的是( )
| A.IBr是双原子分子 |
| B.在很多化学反应中IBr作氧化剂 |
| C.IBr与水反应时,它既是氧化剂,又是还原剂 |
| D.跟NaOH溶液反应可生成NaI和NaBrO |