已知:①lmolH 分子中化学键断裂时需要吸收436 kJ的能量②1 mol C1
分子中化学键断裂时需要吸收436 kJ的能量②1 mol C1 分子中化学键断裂时需要吸收243 kJ的能量③由H原子和C1原子形成l mol HCl分子时释放431 kJ的能量下列叙述中正确的是 ( )
分子中化学键断裂时需要吸收243 kJ的能量③由H原子和C1原子形成l mol HCl分子时释放431 kJ的能量下列叙述中正确的是 ( )
| A.氢气和氯气反应生成氯化氢气体的热化学方程式是: H2( g)+Cl2(g)="2HCl(g)"  |
B.氢气和氯气反应生成2 mol氯化氢气体,反应的 |
C.氢气和氯气反应生成2mol氯化氢气体,反应的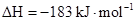 |
D.氢气和氯气反应生成1 mol氯化氢气气体,反应的 |
高炉炼铁过程中发生的反应: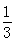 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法不正确的是( )
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法不正确的是( )
| 温度/℃ |
1000 |
1150 |
1300 |
| 平衡常数 |
4.0 |
3.7 |
3.5 |
A.△H<0
B.该反应的平衡常数表达式是K=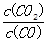
C.其他条件不变,向平衡体系充入CO2气体,K值减小
D.其他条件不变,升高温度,可以降低CO的平衡转化率
下列有关物质的性质和该性质的应用均正确的是( )
| A.常温下浓硫酸能使铝发生钝化,故可在常温下用铝制容器贮藏运输浓硫酸 |
| B.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C.二氧化氯具有还原性,可用于自来水的杀菌消毒 |
| D.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 |
下列陈述中,Ⅰ、Ⅱ都正确且两者间具有因果关系的一组是( )
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
Na2O2使酚酞溶液变红 |
Na2O2能漂白织物、纸浆 |
| B |
SO2可使石蕊溶液先变红后褪色 |
SO2的水溶液具有酸性和漂白性 |
| C |
NH3、HCl可用作喷泉实验 |
NH3、HCl都极易溶于水 |
| D |
晶体硅是良好的半导体材料 |
晶体硅可制作太阳能电池和光导纤维 |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A.常温下,9g H2O中含NA个O–H键 |
| B.1 molFe2+与足量稀硝酸反应,转移3 NA个电子 |
| C.常温常压下,22. 4L SO2和O2的混合气体中含2NA个氧原子 |
| D.0. 1 mol·L–1KAl(SO4)2溶液中含0.2NA个SO42- |
下列条件下,离子能大量共存或者离子方程式正确的是
| A.pH=1的溶液中:Fe2+、ClO-、Na+、SO42- |
| B.在含较多Al3+的溶液中:K+、Cl-、HCO3- |
| C.一小块钠投入到CuSO4溶液中:2Na+Cu2+= Cu+2Na+ |
| D.铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO↑+ 4H2O |