某有机物A的结构简式为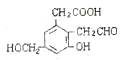 ,若取等质量的A分别与足量的Na、NaOH、新制的Cu(OH)2充分反应,理论上消耗这三种物质的物质的量之比为
,若取等质量的A分别与足量的Na、NaOH、新制的Cu(OH)2充分反应,理论上消耗这三种物质的物质的量之比为
| A.3:2:1 | B.3:2:2 | C.6:4:5 | D.3:2:3 |
下列有机物互为同分异构体的是
①CH2=CHCH3②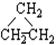 ③CH3CH2CH3④HC
③CH3CH2CH3④HC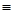 CCH3⑤CH3CH=CHCH2CH3
CCH3⑤CH3CH=CHCH2CH3
| A.①和② | B.①和③ | C.③和④ | D.⑤和③ |
一氯代物的同分异构体有2种,二氯代物的同分异构体有4种的烷烃是
| A.乙烷 | B.丙烷 | C.正丁烷 | D.新戊烷 |
有机物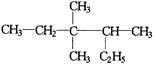 的正确命名为
的正确命名为
| A.2 –乙基– 3,3 –二甲基戊烷 | B.3,3 –二甲基– 4–乙基戊烷 |
| C.3,3,4 –三甲基己烷 | D.3,4,4 –三甲基己烷 |
如图a、b都是惰性电极,通电一段时间后,b极附近溶液呈蓝色。下列说法中不正确的是
| A.U形管中溶液碱性增强 | B.c上析出红色物质 |
| C.a极和Pt都有气泡产生 | D.x是正极,y是负极 |
下列说法不正确的是
| A.同温下,0.1 mol•L-1NH4Cl溶液中NH4+的浓度比0.1 mol•L-1氨水中NH4+的浓度大 |
| B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl多 |
| C.电解饱和食盐水时,阴极得到氢氧化钠溶液和氢气 |
| D.除去溶液中的Mg2+,用OH-比CO效果好,说明Mg(OH)2的溶解度比MgCO3的小 |