过量的NaHCO3和Na2O2混合,在密闭容器中充分混合加热后,最后排出气体,残留的固体是 ( )
| A.Na2O | B.Na2CO3 | C.Na2O2和Na2CO3 | D.Na2O2和Na2O |
右图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,有关Janusene的说法不正确的是: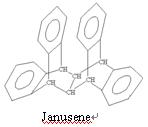
| A.Janusene的分子式为C30H22 |
| B.Janusene属于苯的同系物 |
| C.Janusene苯环上的一氯代物有2种 |
| D.Janusene能使酸性高锰酸钾溶液褪色 |
用U型管作电解池,使用惰性电极,以Na2CO3溶液作电解液,接通直流电源后,阳极和阴极所收集到的气体体积比为(气体经过干燥,并在同温同压下测量)
| A.1︰2 | B.2︰1 | C.略大于1︰2 | D.略大于2︰1 |
标准状况下,将5.6L由CO、CH4、C2H4、C2H2组成的混合气体与18L O2混合于某密闭容器中点燃,反应完成后再恢复到原状况,得CO2气体7.50L,则下列判断正确的是
| A.原混合气体中CO与CH4的体积分数和为33.9% |
| B.原混合气体中,C2H4与C2H2的体积共为1.9L |
| C.反应完成后,生成水的质量为9g |
| D.原混合气体中,CO与CH4的体积比一定为1︰1 |
某苯的同系物的分子式为C11H16,经分析,分子式中除含苯环外(不含其它环状结构),还含有两个“-CH3”、两个“-CH2-”、一个“-CH-”,它的可能结构式有
| A.6种 | B.5种 | C.4种 | D.3种 |
据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为:
HC≡C—C≡C-C≡C-C≡C-C≡N。对该物质判断正确的是
| A.晶体的硬度与金刚石相当 | B.能使酸性高锰酸钾溶液褪色 |
C.不能发生加成反应 |
D.可由乙炔和含氮化合物加聚制得 |