合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应: 。 400℃、30MPa下n(NH3)和n(H2)
。 400℃、30MPa下n(NH3)和n(H2)
随时间变化的关系如图,下列叙述错误的是( )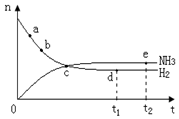
| A.点a的正反应速率比b点的大 |
| B.点c处反应还未达到平衡 |
| C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D.其他条件不变,500℃下反应至t1时刻, n(H2)比图中d点的值大 |
某气态有机物X只含C、H、O三种元素,已知下列条件,现欲确定X的分子式,所需的最少条件是( )
①X中含碳质量分数
②X中含氢质量分数
③X在标准状况下的体积
④质谱确定X的相对分子质量
⑤X的质量
A.①② B.①②④ C.①②⑤ D.③④⑤
设H+的质荷比为β,其有机物样品的质荷比如下图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物可能是( )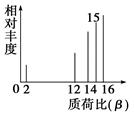
| A.甲醇(CH3OH) | B.甲烷 | C.丙烷 | D.乙烯 |
在核磁共振氢谱图中,只有一个吸收峰的物质是( )
| A.CH3CH2OH | B.HCOOCH3 |
| C.CH3COCH3 | D.CH2=CH—CH3 |
完全燃烧某可燃物2.3 g,只生成4.4 g二氧化碳和2.7 g水,则该可燃物的组成为( )
| A.一定属于烃 |
| B.一定含碳、氢元素,可能含氧元素 |
| C.一定含碳、氢、氧三种元素 |
| D.所含元素大于三种 |
二氟甲烷是性能优异的环保产品,它可替代某些会破坏臭氧层的“氟里昂”产品,用做空调、冰箱和冷冻库等中的制冷剂。试判断二氟甲烷的核磁共振氢谱的峰个数为( )
| A.4 | B.3 | C.2 | D.1 |