铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2  6SO2+Fe3O4,有3 molFeS2参加反应,转移 mol电子。
6SO2+Fe3O4,有3 molFeS2参加反应,转移 mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为 ;从腐蚀废液回收得到金属铜,还需要的试剂是 。
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。
已知:化合物B、C、E中含有两种相同的元素,A可用于玻璃、洗涤剂等的生产,B可用于制作光纤,G的组成元素与D相同。这些化合物之间存在下图所示的转化关系。
请回答:
(1)在化合物A、C、F中含有的 相同元素。
相同元素。
(2)化合物C的化学式为,其水溶液的pH7(填“>”或“<”) 。
。
(3) 700 ℃时,向容积为 2 L的密闭容器中充入一定量的G(g)和H2O(g),发生反应:
2 L的密闭容器中充入一定量的G(g)和H2O(g),发生反应:
G(g)+H2O(g)  D(g)+H2(g)。反应过程中测定的部分数据见下表(表中t1>t2):
D(g)+H2(g)。反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min |
n(G)/mol |
n(H2O)/ mol |
| 0 |
1.20 |
0.60 |
| t1 |
0.80 |
|
| t2 |
0.20 |
① 反应在t1min内的平均速率为v(H2)=mol/(L·min)
② 保持其他条件不变,起始时向容器中充入0.60 mol G和1.20 mol H2O,到达平衡时,
n(D)=mol。
③ 温度升至800℃,上述反应平衡常数为0.64,则正反应为反应(填“放热”或“吸热”)。
下表是短周期中部分元素的原子半径及主要化合价。
| 元素代号 |
W |
R |
X |
Y |
Z |
| 原子半径/nm |
0.037 |
0.157 |
0.066 |
0.070 |
0.077 |
| 主要化合价 |
+1 |
+1 |
-2 |
-3,+5 |
+2,+4 |
请回答:
(1)Z在元素周期表中的位置是,Z单质与Y的最高价氧化物对应水化物的浓溶液反应可生成一种红棕色气体,则反应的化学方程式为。
(2)实验室制取YW3的化学方程式为。
(3)R2X2与W2X反应的离子方程式为,若反应中转移的电子数为0.4×6.02×1023,则参加反应的R2X2的质量为。
(4)X与Z组成一种有臭味的气体,与氧气按物质的量之比为1:2混合后恰好完全燃烧,生成稳定的氧化物,在同温同压下测得燃烧前后气体的总体积不变,则该反应的化学方程式是。
在一定条件下,物质A~E转化关系如下图所示,其中A为单质,常温下E为无色液体。 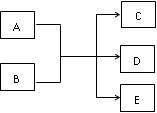
(1)若A、C、D均含氯元素,C为氯碱工业的原料,D的溶液具有漂白性。
①A与B反应的化学方程式是。
②D的溶液可使KI淀粉溶液显蓝色,则D与K I在溶液中反应的离子方程式是
I在溶液中反应的离子方程式是 。
。
③检验C中所含阴离子的实验方法是。
(2)若A为银白色金属,B为某酸的浓溶液。常温下该反应不 能进行,加热后可以发生反应。C可用于做净水剂,D为可形成酸雨的无色气体。C与过量氢氧化钠溶液反应的离子方程式是
能进行,加热后可以发生反应。C可用于做净水剂,D为可形成酸雨的无色气体。C与过量氢氧化钠溶液反应的离子方程式是 。
。
(3)上述(1)、(2)中的D都能使品红溶液褪 色,利用褪色后的溶液探究使其褪色的物质的实验方法是。
色,利用褪色后的溶液探究使其褪色的物质的实验方法是。
(共15分) I写出下列热化学反应方程式
(1)N2 (g)与H2(g)反应生成1molNH3(g),放出46.1KJ热量。
(2)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8KJ热量。
(3)1molC(石墨)与适量H2O(g)反应吸收131.3KJ热量
II .(1)化学反应中均伴随着能量的变化,化学键的断裂和形成是发生能量变化的主要原因。生成物中化学键形成时会__________能量(填“放出”或“吸收”);如果一个化学反应,化学键断裂时的能量变化大于化学键形成时的能量变化,则该反应属于_________反应;如果一个化学反应,反应物的总能量和生成物的总能量有如图所示的关系,则该反应属于__________反应。
(2)不同形式的能量可以相互转换,如:化学能和电能、热能之间的相互转换。如图是一个原电池工作原理的示意图。试回答:
①从能量角度看,它属于____________能转化为____________能;
②装置中Zn为____________极。
右图是一个化学过程的示意图。已知甲池的总反应式为:

(1)请回答下列电极的名称:通入CH3OH的电极名称是,
B(石墨)电极的名称是。
(2)写出电极反应式: 通入O2的电极的电极反应式是。
A(Fe)电极的电极反应式为,
(3)乙池中反应的化学方程式为。