COCl2(g) 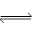 CO(g)+Cl2(g);△H>0 当反应达到平衡时,下列措施能提高COCl2转化率的是:
CO(g)+Cl2(g);△H>0 当反应达到平衡时,下列措施能提高COCl2转化率的是:
①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤ ⑥ ⑥ |
研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质 ,使用时加入水即可放电。关于该电池的下列说法不正确的是
,使用时加入水即可放电。关于该电池的下列说法不正确的是
| A.水既是氧化剂又是溶剂 | B.放电时正极上有 氢气生成 氢气生成 |
| C.放电时OH-向正极移动 | D.总反应为:2Li+2H2O="==" 2LiOH+H2↑ |
能够充分说明在恒温恒容下的密闭容器中反应:2SO2+O2 2SO3,已经达到平衡的标志是
2SO3,已经达到平衡的标志是
| A.容器中SO2、O2、SO3共存 |
| B.容器中SO2和SO3的浓度相同 |
| C.容器中SO2、O2、SO3的物质的量为2︰1︰2 |
| D.容器中压强不随时间的变化而改变 |
下列叙述正确的是
| A.非金属原子间以共价键结合的物质都是共价化合物 |
| B.含有共价键的化合物都是共价化合物 |
| C.凡是能电离出离子的化合物都是离子化合物 |
| D.凡是含有离子键的化合物都是离子化合物 |
已知: 3/2CO2(g)+2Fe(s) = Fe2O3(s)+3/2C(s)△H=-234.1kJ·mol-1
CO2(g) = C(s)+O2(g)△H=+393.4kJ·mol-1。
则2Fe(s)+3/2O2(g)=Fe2O3(s)的△H是
| A.-824.2kJ·mol-1 | B.-627.5kJ·mol-1 |
| C.+861.6kJ·mol-1 | D.+159.3kJ·mol-1 |
在m A(g) + n B(g)  p C(g) + q D(g)的反应中,(m.n.p. q为各物质的化学计量数),经5min达到平衡,测得:A增加3 mol·L-1,B增加1 mol·L-1,C减少2 mol·L-1,此时若给体系加压,平衡不移动,则m :n :p :q为
p C(g) + q D(g)的反应中,(m.n.p. q为各物质的化学计量数),经5min达到平衡,测得:A增加3 mol·L-1,B增加1 mol·L-1,C减少2 mol·L-1,此时若给体系加压,平衡不移动,则m :n :p :q为
| A.2 :3 :2 : 3 | B.2 :2 :3 : 3 |
| C.3 :1 :2 : 2 | D.3 :1 :2 : 3 |