碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容。
(1)右图为元素周期表中的一格,下列说法不正确的是 。
| A.碳元素属于非金属元素 |
| B.碳原子核内质子数为6 |
C.碳元素的原子结构示意图为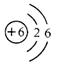 |
| D.碳的相对原子质量为12.01 |
(2)煤、 和天然气常称为化石燃料。汽车使用天然气作燃料,排放污染物较少,写出天然气燃烧的化学方程式 。
(3)“低碳生活”倡导低能耗、低污染、低排放,主要是为了减少 (填化学式)的排放量。下列做法符合“低碳经济”的是 。
①提倡发送电子贺卡 ②大力发展火力发电 ③研制和开发新能源
④提倡使用一次性木筷 ⑤增强室内自然采光
(4)二氧化碳和氨气(NH3)在高温、高压下反应,生成尿素[CO(NH2)2]和水,反应的化学方程式是 。
我国自主设计的大型客机成功试飞,首艘国产航母正式下水,标志着我国的合金制造技术取得重大突破。根据所学知识回答问题。
(1)生铁和钢都是铁的合金,其中含碳量较高的是 。
(2)探究Al与酸的反应前,用砂纸打磨铝条,是为了除去 (填化学式)。
(3)某合金中含有金属钪(Sc)。相同条件下,取相同状态的金属钪和锌分别与相同浓度的盐酸反应,钪产生气泡速率明显更快,则金属活动性Sc Zn(填“>”或“<”)。根据上述结论,下列说法不正确的是 (填序号)。
A.将Sc投入CuSO4溶液中有红色物质析出
B.仅用Fe(NO3)2溶液、Sc(NO3)3溶液、Ag能验证钪和铁的活动性强弱
C.仅用Fe、Sc、稀H2SO4溶液能验证钪和铁的活动性强弱
(4)已知Sc与稀盐酸发生置换反应,生成+3价化合物。写出该反应的化学方程式 。
老师要求用规定量的BaCl2溶液与适量的Na2SO4溶液制备BaSO4.完成操作I后,丁丁发现自己错把Na2CO3溶液当成Na2SO4溶液,而此时BaCl2溶液已完全消耗。老师启发他,可用生成物和其他试剂完成制备BaSO4的实验。整个实验流程如图所示:

(1)反应②的化学方程式为 ,溶液b中的溶质有 。
(2)反应③的基本反应类型为 。
(3)操作Ⅱ的名称为 。
(4)从理论上讲,该实验过程最终得到的BaSO4质量与原方案得到的BaSO4质量是否相等? (填“是”或“否”)
某课外活动中,学生利用如图所示的杠杆完成探究实验,杠杆已调至平衡。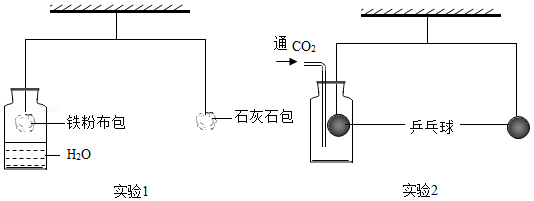
(1)实验1中,较长时间后,左边铁粉布包下降,是因为铁粉与 发生了反应。将铁粉换成下列物质中的 (填序号),杠杆也会出现相似现象。
A.NaCl
B.NaOH
C.CaO
(2)实验2中,通入CO2一段时间,右边乒乓球 (填“上升”或“下降”)。再往集气瓶中滴入足量NaOH溶液,杠杆重新平衡,发生反应的化学方程式为 。
重庆是座美丽的城市,有丰富的旅游资源。根据所学知识回答下列问题。
(1)火锅是重庆的旅游名片,下列火锅菜品中富含蛋白质的是 (填序号)。
A.土豆片
B.莴笋尖
C.鹌鹑蛋
D.苕粉条
(2)某些景点的观光汽车使用乙醇汽油作为燃料,可以减少尾气污染。写出乙醇(C2H5OH),完全燃烧的化学方程式 。
(3)乘船游览江景是重庆旅游的一大特色。游船上使用的下列物品中,用合成材料制成的是 (填序号)。
A.铝合金护栏
B.塑料救生衣
C.真皮椅套
D.钢制甲板
海水中含有钙、镁、氯、硫等元素。
(1)上述元素中 (填符号)是人体内含量最高的金属元素。
(2)硫原子的结构示意图为 ,则S2﹣的电子数为 。
,则S2﹣的电子数为 。
(3)海水有苦味,是因为含有氯化镁,其化学式为 。