氧化还原反应中,水的作 用可以是氧化剂、还原剂、既是氧化剂又是还
用可以是氧化剂、还原剂、既是氧化剂又是还 原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是
原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是
| A.2Na2O2+2H2O=4NaOH+O2↑ |
| B.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| C.4NO2+O2+2H2O=4HNO3 |
| D.2Al+2NaOH+2H2O=2NaAlO2+3H2↑ |
有机物的结构可用键线式表示,如CH2=CHCH2Br可表示为 。下列关于两种有机化合物A和B的说法中错误的是
。下列关于两种有机化合物A和B的说法中错误的是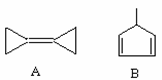
| A.有机物A分子所有碳原子均在同一平面上 |
| B.有机物B的化学式为C6H8 |
| C.有机物A的二氯取代产物有4种 |
| D.等物质的量的A和B与H2完全加成消耗H2的量相同 |
有关 分子结构的下列叙述中,正确的是
分子结构的下列叙述中,正确的是
| A.除苯环外的其余碳原子有可能都在一条直线上 |
| B.所有的原子都在同一平面上 |
| C.12个碳原子不可能都在同一平面上 |
| D.12个碳原子有可能都在同一平面上 |
【改编】下列物质中遇氯化铁溶液显紫色的是
下列有机化合物的分类不正确的是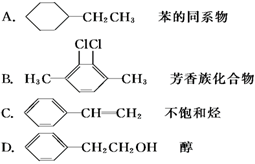
【改编】一定温度下,反应 N2(g) + O2(g) 2NO(g)在密闭容器中进行,下列措施能使化学反应速率减慢的是
2NO(g)在密闭容器中进行,下列措施能使化学反应速率减慢的是
| A.缩小体积使压强增大 | B.恒容,充入N2 |
| C.恒容,充入H2 | D.恒压,充入H2 |