下列事实能用同一原理解释的是
| A.SO2、Cl2均能使品红溶液褪色 |
| B.NH4HCO3晶体、固体I2受热均能变成气体 |
| C.S与Fe、Cu反应均生成低价硫化物 |
| D.ClO-与S2-或H+均不能共存 |
已知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点就越高。则下列溶液沸点最高的是
| A.0.01 mol·L-1的蔗糖溶液 | B.0.01 mol·L-1的CaCl2溶液 |
| C.0.02 mol·L-1的NaCl溶液 | D.0.02 mol·L-1的CH3COOH溶液 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.常温下,1L 1mol·L-1的NH4NO3溶液中氮原子数为2NA |
| B.1mol羟基中电子数为10NA |
| C.在反应中,每生成3mol I2转移的电子数为6NA |
| D.常温常压下,22.4L乙烯中C−H键数为4NA |
某硫原子的质量是a g, 12C原子的质量是b g,若NA只表示阿伏加德罗常数的数值,则下列说法中正确的是
①该硫原子的相对原子质量为
②m g该硫原子的物质的量为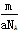 mol
mol
③该硫原子的摩尔质量是aNA g
④ag该硫原子所含的电子数为16NA
| A.①③ | B.②④ | C.①② | D.②③ |
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.4.0 g重水(D2O)中所含质子数为0.4NA |
| B.4.48 L N2与CO的混合物中所含分子数为0. 2NA |
| C.6.2 g白磷与红磷的混合物中所含磷原子数为0.2NA |
| D.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
下列物质分类正确的是
| A.SO2、SiO2、CO均为酸性氧化物 |
| B.稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C.烧碱、冰醋酸、四氯化碳均为电解质 |
| D.福尔马林、水玻璃、氨水均为混合物 |