用特殊方法把固体物质加工到纳米级(1-100nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是
| A.溶液 | B.悬浊液 | C.胶体 | D.乳浊液 |
高温下2HBr(g) H2(g)+Br2(g) △H>0, 达到平衡时,要使混合气体颜色加深,可采取的方法
H2(g)+Br2(g) △H>0, 达到平衡时,要使混合气体颜色加深,可采取的方法
| A.降低温度 | B.缩小体积 | C.减小压强 | D.增大H2浓度 |
1g H2燃烧生成液态水放出142.9 kJ的热量,下列热化学方程式书写正确的是( )
| A.2H2(g)+ O 2(g) = 2H2O (1), ΔH = —142.9 kJ·mol-1 |
| B.2H2(g)+ O 2(g) = 2H2O (1), ΔH = —571.6 kJ·mol-1 |
| C.2H2+O2 = 2H2O, ΔH = —571.6 kJ·mol-1 |
| D.H2(g)+ O 2(g) = H2O (1), ΔH = +285.8 kJ·mol-1 |
下列化学反应ΔH最大的是
| A.NaOH(aq)+HCl(aq)=NaCl(aq )+H2O(l);△H1 |
B.NaOH(aq)+ H2SO4(aq)= H2SO4(aq)= Na2SO4(aq)+H2O(l);△H2 Na2SO4(aq)+H2O(l);△H2 |
| C.CH3COOH(aq)+NaOH(aq)=CH3COONa (aq )+H2O(l);△H3 |
D.NaOH(aq)+ H2SO4(浓)= H2SO4(浓)= Na2SO4(aq)+H2O(l);△H4 Na2SO4(aq)+H2O(l);△H4 |
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):根据以上规律判断,下列结论正确的是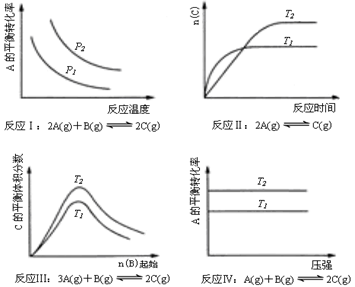
| A.反应Ⅰ:△H>0,P2>P1 | B.反应Ⅱ:△H<0,T1>T2 |
| C.反应Ⅲ:△H>0,T2<T1 | D.反应Ⅳ:△H<0,T2>T1 |
将2mol SO2和2mol SO3气体混合于固定容积的容器内,在一定条件下,发生反应:2SO2 + O2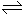 2SO3,达平衡时SO3为n mol。相同温度下分别按下列配比,平衡后SO3的物质的量大于n mol的是
2SO3,达平衡时SO3为n mol。相同温度下分别按下列配比,平衡后SO3的物质的量大于n mol的是
| A.2mol SO2和1mol O2 |
| B.2mol SO2和1mol O2和2mol SO3 |
| C.4mol SO2和1mol O2 |
| D.3mol SO2和0.5mol O2和1mol SO3 |