一定温度下,在2L的密闭容器中加入4mol A和6mol B,发生如下反应:
2A(g)+3B(g) 4C(g)+D(g)反应10min后达平衡,此时D的浓度为0.5mol/L。下列说法正确的是
4C(g)+D(g)反应10min后达平衡,此时D的浓度为0.5mol/L。下列说法正确的是
A、前10min反应的平均速率V(C)=0.10mol/L·min
B、10min后向容器中加入A,重新平衡时 A的转化率一定大于50%
A的转化率一定大于50%
C、恒温下将反应容器体积缩小一半,则D的平衡浓度小于1.0mol/L
D、反应达平衡时B的平衡浓度是1.5mol/L
P单质在反应4P+3KOH+3H2O=3KH2PO2+PH3中的变化是
| A.被氧化 | B.被还原 |
| C.既被氧化又被还原 | D.既未被氧化又未被还原 |
质量相同的两种气体A、B,在同温、同压下,A的密度小于B的。下列说法错误的是
A.A占的体积比B大 B.A的分子数比B多
C.A的摩尔质量比B大 D.A的物质的量比B大
下列叙述不正确的是
| A.虽然石墨有较好的导电性,但它不属于电解质 |
| B.CaCO3、BaSO4都难溶于水,但它们都是电解质 |
| C.酒精(纯净物)在水溶液和熔融状态下均不能导电,所以酒精属于非电解质 |
| D.实验测定液态HCl、固体KNO3均不能导电,所以HCl、KNO3均是非电解质 |
下列各组反应,前后均可以用同一个离子方程式表示的是
| A.HCl+Na2CO3 HCl+NaHCO3 |
| B.HCl+Na2CO3 H2SO4+K2CO3 |
| C.H2S+NaOHH2SO4+KOH |
| D.BaCl2+Na2SO4 BaCO3+H2SO4 |
下列关于物质的量浓度表述正确的是
A.0.2mol·L-1Na2SO4溶液中含有Na+和SO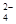 总物质的量为0.6mol 总物质的量为0.6mol |
| B.50mL2mol·L-1NaCl溶液和100mL0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度相等 |
| C.用1L水吸收22.4L氯化氢所得盐酸的浓度是1mol·L-1 |
| D.10g98%的硫酸(密度为1.84g·cm-3)与10mL18.4mol·L-1的硫酸的浓度是相同的 |