对水垢的主要成分是CaC03和Mg(OH)2而不是CaC03和MgC03的原因解释,其中正确的有
| A.Mg(OH)2的溶度积大于MgC03的溶度积,且在水中发生了沉淀转化 |
| B.Mg(OH)2的溶度积小于MgC03的溶度积,且在水中发生了沉淀转化 |
C.MgCO3电离出的 -发生水解,使水中 -发生水解,使水中 -浓度减小,对Mg(OH)2的沉淀溶解平衡而言,Qc<Ksp,生成Mg(OH)2沉淀 -浓度减小,对Mg(OH)2的沉淀溶解平衡而言,Qc<Ksp,生成Mg(OH)2沉淀 |
| D.MgCO3电离出的CO32-发生水解,使水中OH-浓度增大,对Mg(OH)2的沉淀溶解平衡而言,Qc> Ksp,生成Mg(OH)2沉淀 |
下列各项与反应热的大小无关的是
| A.反应物和生成物的状态 | B.反应物量的多少 |
| C.反应物的性质 | D.反应的快慢 |
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知:3I2+6OH-=IO+5I-+3H2O,下列说法不正确的是( )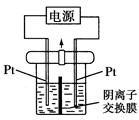
| A.右侧发生的电极反应式:2H2O+2e-=H2↑+2OH- |
| B.电解结束时,右侧溶液中含有IO3- |
C.电解槽内发生反应的总化学方程式:KI+3H2O KIO3+3H2↑ KIO3+3H2↑ |
| D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学反应不变 |
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入( )
| A.0.15 mol CuO | B.0.1 mol CuCO3 |
| C.0.075mol Cu(OH)2 | D.0.05 mol Cu2(OH)2CO3 |
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂溶解在亚硫酰氯(SOCl2)中形成,电池的总反应式为8Li+3SOCl2=6LiCl+Li2SO3+2S,则下列叙述正确的是 ( )
| A.用该电池电解CuCl2溶液产生2.24LCl2时,有0.2mol电子转移 |
| B.金属锂作电池的负极,石墨作电池的正极,加入硫酸可提高电解质的导电性 |
| C.电池工作(放电)过程中,SOCl2被还原为Li2SO3 |
| D.电池工作过程中,负极消耗的锂与正极生成的硫质量之比为7:8 |
反应mA(g)+ nB(g) 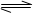 pC(g)+qD(g),经5min后达到平衡,测得此时A的浓度减少了a mol/L,同时C的浓度增加了2a/3 mol/L,又测得平均反应速率v(C)=2v(B)。达到平衡后,若保持温度不变,给体系加压,平衡不移动,那么该反应可表示为()
pC(g)+qD(g),经5min后达到平衡,测得此时A的浓度减少了a mol/L,同时C的浓度增加了2a/3 mol/L,又测得平均反应速率v(C)=2v(B)。达到平衡后,若保持温度不变,给体系加压,平衡不移动,那么该反应可表示为()
A.2A(g)+ 6B(g)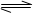 3C(g)+5D(g)B.3A(g)+ B(g)
3C(g)+5D(g)B.3A(g)+ B(g)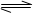 2C(g)+2D(g)
2C(g)+2D(g)
C.3A(g)+ B(g) 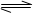 2C(g)+ D(g) D.A(g)+ 3B(g)
2C(g)+ D(g) D.A(g)+ 3B(g)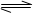 2C(g)+2D(g)
2C(g)+2D(g)