下列离子方程式书写正确的是
| A.向明矾溶液中加入过量的氢氧化钡溶液: Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
| B.用食醋除去水瓶中的水垢:CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O |
| C.向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+=Fe2++2H2O |
| D.向次氯酸钠溶液中通入少量二氧化硫:2ClO-+ SO2 + H2O = SO32- + 2HClO |
(10分)现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m+n_________p(填“>”“=”“<”)。
(2)减压时,A的质量分数_________。(填“增大”“减小”或“不变”;下同)
(3)若加入B(体积不变),则A的转化率______。
(4)若加入催化剂,平衡时气体混合物的总物质的量___
反应N2(g)+O2(g) 2NO(g)在恒容密闭容器中进行,达到平衡后,充入N2,下列说法正确的是
2NO(g)在恒容密闭容器中进行,达到平衡后,充入N2,下列说法正确的是
| A.平衡向逆反应方向移动,N2和O2的转化率都减小 |
| B.平衡向正反应方向移动,N2和O2的转化率都增大 |
| C.压强增大平衡不移动,N2的转化率不变 |
| D.平衡向正反应方向移动,N2的转化率减小,O2的转化率增大 |
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?) aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是
aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是
| A.若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅱ>Ⅰ |
| B.若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ |
| C.若X为固态,Y为气态,则Ⅰ、Ⅱ中从起始到平衡所需时间相同 |
| D.平衡时Ⅰ容器的体积小于V L |
在密闭容器中发生反应:aX(g)+bY(g) cZ(g)+dW(g),达到平衡后,保持温度不变,将气体压缩到原来的一半体积,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述不正确的是
cZ(g)+dW(g),达到平衡后,保持温度不变,将气体压缩到原来的一半体积,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述不正确的是
| A.a+b>c+d | B.平衡向逆反应方向移动 |
| C.Z的体积分数减小 | D.X的转化率下降 |
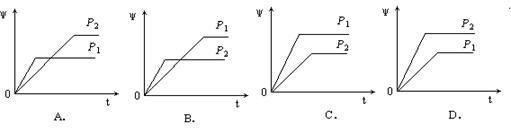
在一定温度不同压强(P1<P2)下,可逆反应:2X(g)  2Y(g) + Z(g) 中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是
2Y(g) + Z(g) 中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是