大气污染是指
| A.大气中含有少量的有毒、有害的物质 |
| B.大气中有毒、有害的物质可以自净到正常值 |
| C.大气中某些有毒、有害物质的含量超过正常值或大气的自净能力 |
| D.空气中氮气的含量大于氧气的含量 |
工业上常用还原沉淀法处理含铬废水(Cr2O72—和CrO42—),其流程为:
已知:
(1)步骤①中存在平衡:2Cr O42—(黄色)+2H+ Cr2O42—(橙色)+H2O
Cr2O42—(橙色)+H2O
(2)步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH 一(aq)
Cr3+(aq)+3OH 一(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol·L-1时可视作该离子不存在下列有关说法中,正确的是:()
| A.步骤①中加酸,将溶液的pH 调节至2,溶液显黄色,CrO42—离子浓度增大 |
B.步骤①中当2v(CrO42 一)=v(Cr2O72—)时,说明反应2CrO42—(黄色)+2H+ Cr2O72—(橙色)+H2O 达到平衡状态 Cr2O72—(橙色)+H2O 达到平衡状态 |
| C.步骤②中,若要还原1 mol Cr2O72一离子,需要12 mol(NH4)2Fe(SO4)2·6H2O。 |
| D.步骤③中,当将溶液的pH 调节至6 时,则可认为废水中的铬已除尽 |
下列说法正确的是:()
A.反应A(g) 2B(g);△H,若正反应的活化能为Ea kJ mol-1,逆反应的活化能为Eb kJ·mol-1,则△H=(Ea-Eb)kJ·mol-1 2B(g);△H,若正反应的活化能为Ea kJ mol-1,逆反应的活化能为Eb kJ·mol-1,则△H=(Ea-Eb)kJ·mol-1 |
| B.已知25℃时,有关弱酸的电离平衡常数:HCN Ka=4.9×10-10; H2CO3 Ka1=4.3×10-7,Ka2=5.6×10-11。则CO2通入NaCN溶液中反应的化学方程式为:2NaCN+H2O+CO2=2HCN+Na2CO3 |
C.已知: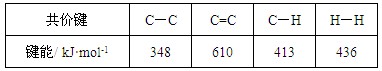 则反应 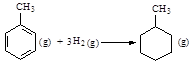 的焓变为ΔH = -384 kJ·mol-1 的焓变为ΔH = -384 kJ·mol-1 |
| D.一定浓度的NaOH溶液,温度升高PH值不变 |
下列说法正确的是:()
A.按系统命名法,有机物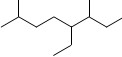 可命名为3,7-二甲基-4-乙基辛烷 可命名为3,7-二甲基-4-乙基辛烷 |
B.已知Ka是平衡常数,PKa=-lgKa 则下图所示有机物1mol最多能消耗3molNaOH 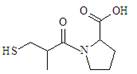 |
C. 分子中所有原子共平面 分子中所有原子共平面 |
| D.碳原子数小于或等于8的单烯烃,与HBr加成反应的产物只有一种结构,符合条件的单烯烃有6种 |
如图是一种可充电的锂离子电池充、放电的工作示意图。放电时该电池的电极反应式为:
负极:LixC6-xe-=C6+xLi+(LixC6表示锂原子嵌入石墨形成的复合材料)
正极:Li1-xMnO2+xLi++x e-=LiMnO2(LiMnO2表示含锂原子的MnO2)
下列有关说法正确的是:()
A.该电池的反应式为Li1-xMnO2+LixC6 LiMnO2+C6 LiMnO2+C6 |
| B.在整个充电或放电过程中都只存在一种形式的能量转化 |
| C.K与N相接时,Li+由A极区迁移到B极区 |
| D.K与M相接时,A是阳极,发生氧化反应 |
X、Y、Z和W代表原子序数依次增大的四种短周期主族元素,它们满足以下条件:①在元素周期表中,Z与Y、W均相邻;②X、Y、W分别位于不同周期;③Y、Z、W三种元素的原子最外层电子数之和为17。下列说法正确的是:()
| A.四种元素的原子半径由小到大的顺序为:r(X)<r(Y)<r(Z)<r(W) |
| B.X、Y、Z既能形成离子化合物,又能形成共价化合物 |
| C.X与其余三种元素之间形成的核外电子总数为10的微粒只有4种 |
| D.H2Z的熔点比H2W高,是因为它们的晶体类型不同 |