下列说法不正确的是
| A.已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 |
B.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,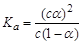 。若加入少量醋酸钠固体,则CH3COOH 。若加入少量醋酸钠固体,则CH3COOH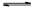 CH3COO-+H+向左移动,α减小,Ka变小 CH3COO-+H+向左移动,α减小,Ka变小 |
| C.0.1 mol·L-1的碳酸钠溶液的pH大于0.1 mol·L-1的醋酸钠溶液的pH |
D.已知:Fe2O3(s)+3C (石墨) (石墨) 2Fe(s)+3CO(g),△H=+489.0 kJ/mol。 2Fe(s)+3CO(g),△H=+489.0 kJ/mol。 |
CO(g)+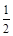 O2(g)
O2(g) CO2(g),△H=-283.0 kJ/mol。
CO2(g),△H=-283.0 kJ/mol。
C(石墨)+O2(g) CO2(g),△H=-393.5 kJ/mol。
CO2(g),△H=-393.5 kJ/mol。
则4Fe(s)+3O2(g) 2Fe2O3(s),△H=-1641.0 kJ/mol
2Fe2O3(s),△H=-1641.0 kJ/mol
下列离子方程式的书写正确的是
| A.实验室用大理石和稀盐酸制取CO2:2H++CO32— =CO2↑+H2O |
| B.实验室用二氧化锰和浓盐酸制取Cl 2:MnO2+4HCl (浓)=Mn2++ Cl 2↑+2H2O+ 2C1- |
| C.C12与NaOH溶液反应:Cl2+OH-=C1-+C1O-+H2O |
| D.实验室用硅酸钠溶液和稀盐酸制取硅酸胶体:2H++SiO32-=H2SiO3(胶体) |
下列属于放热反应的是
| A.C+CO2 | B.Ba(OH)2·8H2O+NH4Cl(固体) |
| C.KClO3受热分解 | D.CaO+H2O |
在指定条件下能够大量共存的一组离子是
| A.在pH=13的溶液中:Na+、Ba2+、Cl-、NO3- |
| B.使石蕊试液变红的溶液:Na+、ClO-、Cl-、NO3- |
| C.无色溶液: Cu2+、K+、SO42-、Cl- |
| D.强碱性溶液:K+、Mg2+、NO3-、HCO3- |
把下列物质分别加入装有水的锥形瓶里立即塞紧U形管的塞子,已知U形管内预先装有少量水(为使水容易观察,预先染成红色)。如图所示,结果U型管右边液面升高,则加入的物质可能是①NaOH固体 ②浓H2SO4 ③NH4NO3晶体 ④Na2O2 ⑤生石灰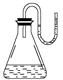
| A.①②④⑤ | B.①②③ | C.②③⑤ | D.③④⑤ |
下列各组粒子,核外电子总数和质子总数均相同的是
| A.S2-和HS- | B.H3O+和OH- | C.Na+和NH4+ | D.K+和Ne |