把锌片和铁片放在盛有食盐水和酚酞的表面皿中,如图所示。最先观察到酚酞变红的现象的区域是( )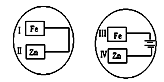
| A.II和IV | B.II和III | C.I和IV | D.I和III |
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(v)与时间(t)关系如右图。反应中镁和铝的
| A.物质的量之比为3:2 | B.质量之比为3:2 |
| C.摩尔质量之比为2:3 | D.反应速率之比为2:3 |
下列说法中,正确的是
| A.工业上制备镁是用电解饱和氯化镁水溶液来完成的 |
| B.硅的化学性质不活泼,在自然界中可以以游离态存在 |
| C.Na2O和Na2O2组成元素相同,且都能与硫酸溶液反应 |
| D.SO2通入新制氯水中,氯水褪色是因为SO2具有漂白性 |
下列叙述I和II均正确并且有因果关系的是
| 选项 |
叙述I |
叙述II |
| A |
相同条件下NaHCO3的溶解度比Na2CO3的小 |
向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊 |
| B |
钠比铜的金属性强 |
金属钠可从硫酸铜溶液中置换出铜单质 |
| C |
常温下铝与浓硫酸、浓硝酸均不反应 |
可用铝槽车密封运送浓硫酸、浓硝酸 |
| D |
合成氨反应为吸热反应 |
该反应需在高温条件下进行 |
下列图示与对应的叙述相符的是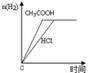
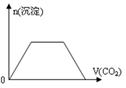
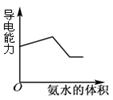

图1图2图3图4
| A.图1表示向等体积、等物质的量浓度的盐酸和醋酸溶液中,分别加入足量镁粉 |
| B.图2表示向Ba(OH)2、KAlO2混合溶液中通入CO2 |
| C.图3表示表示向盐酸和醋酸混合溶液中滴入氨水 |
| D.图4表示在含等物质的量NaHCO3、Na2CO3的混合溶液中滴加0.1mol·L-1盐酸至过量时,产生气体的体积与消耗盐酸的关系 |
下列叙述中正确的是
| A.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| B.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| C.液溴易挥发,在存放液溴的试剂瓶中应加水封 |
| D.硝酸亚铁溶液中要加入稀硝酸抑制水解,防止溶液变浑浊 |