向明矾溶液中逐渐滴加Ba(OH)2溶液,符合要求的离子方程式为
| A.加入过量的Ba(OH)2溶液时:2Al3++3SO42-+3Ba2++6OH—= 2Al(OH)3↓+3BaSO4↓ |
| B.溶液恰好呈中性时:2Al3++3SO42-+3Ba2++6OH— = 2Al(OH)3↓+3BaSO4↓ |
| C.SO42-离子恰好完全沉淀时:Al3++SO42-+Ba2++4OH— = AlO2-+BaSO4↓+2H2O |
| D.明矾与Ba(OH)2按物质的量比1∶1反应时:Al3++SO42-+Ba2++3OH—= Al(OH)3↓+BaSO4↓ |
下列说法或表示法正确的是( )
| A.测定HCl和NaOH的中和热时,每次实验均应测量三个温度,即盐酸起始温度、NaOH起始温度和反应后的终止温度 |
| B.由“C(石墨)=C(金刚石);△H=" +119" kJ/mol ”可知金刚石比石墨稳定 |
| C.在稀溶液中: H++OH-=H2O;△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量等于57.3kJ |
| D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l);△H= +285.8kJ/mol |
据美国《科学》杂志报道,外太空的某个星球的大气层中含有大量的CH2=CHOH,此物质常温下为液体,不稳定,易转化为CH3CHO,化学方程式为CH2=CHOH CH3CHO△H<0。据此,以下叙述中,不正确的是()
CH3CHO△H<0。据此,以下叙述中,不正确的是()
| A.该星球表面温度很低 |
| B.低温下稳定性:CH2="CHOH" < CH3CHO |
| C.该星球表面温度很高 |
| D.高温下稳定性:CH2="CHOH" > CH3CHO |
一种气态烷烃和一种气态烯烃,它们分子里的碳原子数相同。将1.0体积这种混合气体在氧气中充分燃烧,生成2.0体积的CO2和2.4体积的水蒸汽(气体体积均在相同状况下测定)。则混合气中烷烃和烯烃的体积比为 ( )
( )
| A.3﹕1 | B.1﹕3 | C.2﹕3 | D.3﹕2 |
甲基叔丁基醚是一种难溶于水的物质,可用作无铅汽油的添加剂。用以下2种方案可制得甲基叔丁基醚:
方案甲: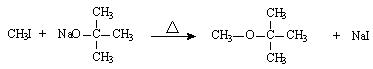
方案乙: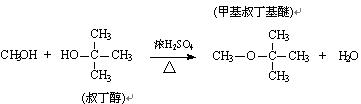
针对上述2种方案,下列说法错误的是 ( )
( )
| A.2种实验方案中,方案乙制得的产物更纯净,有利于分离 |
| B.甲方案中得到的2种产物可用水洗分液法分离 |
| C.甲基叔丁基醚一溴代物有2种 |
| D.若甲基叔丁基醚含有的叔丁醇,可用金属钠除去 |
化合物丙由如下反应得到: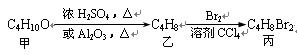
丙的结构简式不可能是 ( )
( )
| A.CH3CH2CHBrCH2Br | B.CH3CH(CH2Br)2 |
| C.CH3CHBrCHBrCH3 | D.(CH3)2CBrCH2Br |