Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的物质的量之比为1∶1时,实际参加反应的Cu2S与HNO3的物质的量之比为
| A.1∶7 | B.1∶9 | C.1∶5 | D.2∶9 |
已知:298K时,2SO2(g) + O2(g)  2SO3(g);△H = —Q1 KJ/mol,在相同温度下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q2KJ,则下列关系式正确的是
2SO3(g);△H = —Q1 KJ/mol,在相同温度下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q2KJ,则下列关系式正确的是
| A.无法比较 | B.Q1<Q2 | C.Q1=Q2 | D.Q1>Q2 |
下列热化学方程式书写正确的是
| A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g); △H=-1367.0 kJ/mol(燃烧热) |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=+57.3kJ/mol(中和热) |
| C.S(s)+O2(g)=SO2(g); △H=-296.8kJ/mol(反应热) |
| D.2NO2=O2+2NO; △H=+116.2kJ/mol(反应热) |
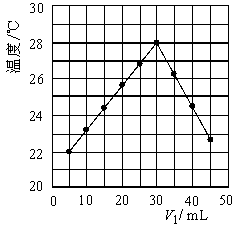
将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是
| A.做该实验时环境温度为22 ℃ |
| B.该实验表明化学能可以转化为热能 |
| C.NaOH溶液的浓度约是1.00 mol/L |
| D.该实验表明有水生成的反应都是放热反应 |
25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是
| A.2H2(g)+O2(g)=2H2O(1)△H= ―285.8kJ/mol |
| B.2H2(g)+ O2(g)=2H2O(1)△H=" +571.6" kJ/mol |
| C.2H2(g)+O2(g)=2H2O(g)△H=" ―571.6" kJ/mol |
D.H2(g)+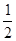 O2(g)=H2O(1)△H = ―285.8kJ/mol O2(g)=H2O(1)△H = ―285.8kJ/mol |
下列说法中正确的是
| A.在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| B.生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时,反应为吸热反应 |
| C.反应产物的总焓大于反应物的总焓时,反应吸热,ΔH>0 |
| D.ΔH的大小与热化学方程式的计量系数无关 |