现有四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是( )
| A.第一电离能:③>②>① |
| B.原子半径:③>②>① |
| C.电负性:③>②>① |
| D.最高正化合价:③>②>① |
某碳氢化合物分子的结构式如图: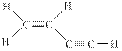 ,下列有关该分子的叙述正确的是()
,下列有关该分子的叙述正确的是()
| A.该分子含5个σ键,3个π键 | B.该分子是非极性分子 |
C.该分子的碳原子均是以 sp2杂化轨道参与成键 sp2杂化轨道参与成键 |
D.分子中有4个原子在同一直线上 |
科学家新发现的两种分子COS和C3O2(均为新型可燃性碳的化合物)的结构式分别为 和
和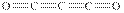 ,则下列有关说法正确的是()
,则下列有关说法正确的是()
| A.C3O2和COS在氧气中完全燃烧的产物均是CO2 |
| B.CO、C3O2、CO2中碳元素的化合价依次升高 |
| C.COS和C3O2均是含极性键的非极性分子 |
D.CO2、COS、C3O2三分子中碳原子均采取 杂化 杂化 |
磷化硼是一种超硬耐磨涂层材料,右图为其晶胞,其中的每个原子均满足8电子稳定结构。
下列有关说法正确的是()
| A.磷化硼晶体的熔点很低 |
| B.磷化硼晶体的化学式为BP,属于离子晶体 |
C.磷化硼晶体中 每个原子 每个原子 均形成4条共价键 均形成4条共价键 |
| D.磷化硼晶体结构中微粒的空间堆积方式与氯化钠相同 |
据最新报道,科学家发现了如下反应:O2 + PtF6 O2[PtF6],已知O2[PtF6]为配位化合物(其中Pt为+5价),对于此反应,下列说法正确的是()
O2[PtF6],已知O2[PtF6]为配位化合物(其中Pt为+5价),对于此反应,下列说法正确的是()
| A.该配合物的配位原子是F和O,配位数为8 | B.在此反应中,O2是氧化剂,PtF6是还原剂 |
| C.O2[PtF6]中Pt与F之间以离子键相结合 | D.反应中每生成1mol O2[PtF6],转移1 mol电子 |
原子序数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,核内质子数为2n2-1。下列有关X的说法中不正确的是()
| A.X原子的最外层电子数和核电荷数肯定为奇数 | B.X可能形成化学式为KXO3的含氧酸钾盐 |
| C.X能形成化学式为X(OH)3的碱 | D.X能与某些金属元素形成离子化合物 |