将等物质的量浓度、等体积的硫酸与烧碱溶液混合后,滴入紫色石蕊试液,溶液呈( )
| A.紫色 | B.红色 | C.蓝色 | D.无色 |
常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
2Fe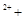 H2O2
H2O2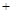 2H
2H → 2Fe
→ 2Fe 2H2O 2Fe
2H2O 2Fe H2O2 → 2Fe
H2O2 → 2Fe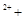 O2↑
O2↑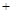 2H
2H
下列说法正确的是( )
A.H2O2的氧化性比Fe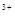 强,其还原性比Fe 强,其还原性比Fe 弱 弱 |
| B.在H2O2分解过程中,溶液的pH逐渐下降 |
C.在H2O2分解过程中,Fe 和Fe 和Fe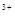 的总量保持不变 的总量保持不变 |
D.H2O2生产过程要严格避免混入Fe |
水是最宝贵的资源之一。下列表述正确的是( )
A.H2O的电子式为 |
B.4℃时,纯水的pH |
| C.D216O中,质量数之和是质子数之和的两倍 |
| D.273K、101kPa,水分子间的平均距离d:d(气态)>d(液态)>d(固态) |
已知: ,如果要合成
,如果要合成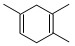 所用的原始原料可以是( )
所用的原始原料可以是( )
| A.2-甲基-l, 3-丁二烯和2-丁炔 | B.1, 3-戊二烯和2-丁炔 |
| C.2, 3-二甲基-1, 3-戊二烯和乙炔 | D.2, 3-二甲基-l, 3-丁二烯和丙炔 |
如图,采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率,反应原理为:NO(g) NO2(g)
NO2(g) 2NH3(g)
2NH3(g) 2N2(g)
2N2(g) 3H2O(g),相关说法正确的是 )
3H2O(g),相关说法正确的是 )
| A.上述反应的正反应为吸热反应 |
| B.催化剂①、②分别适合于250℃和450℃左右脱氮 |
| C.曲线①、②最高点表示此时平衡转化率最高 |
| D.相同条件下,改变压强对脱氮率没有影响 |
将amol钠和amol铝一同放入mg水(足量)中,所得溶液的密度为dg/mL,该溶液的质量百分比浓度为( )
A.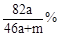 |
B.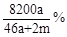 |
C.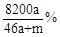 |
D.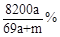 |